9.4 Sel Elektrolitik
Definisi dan Konduktor Elektrik
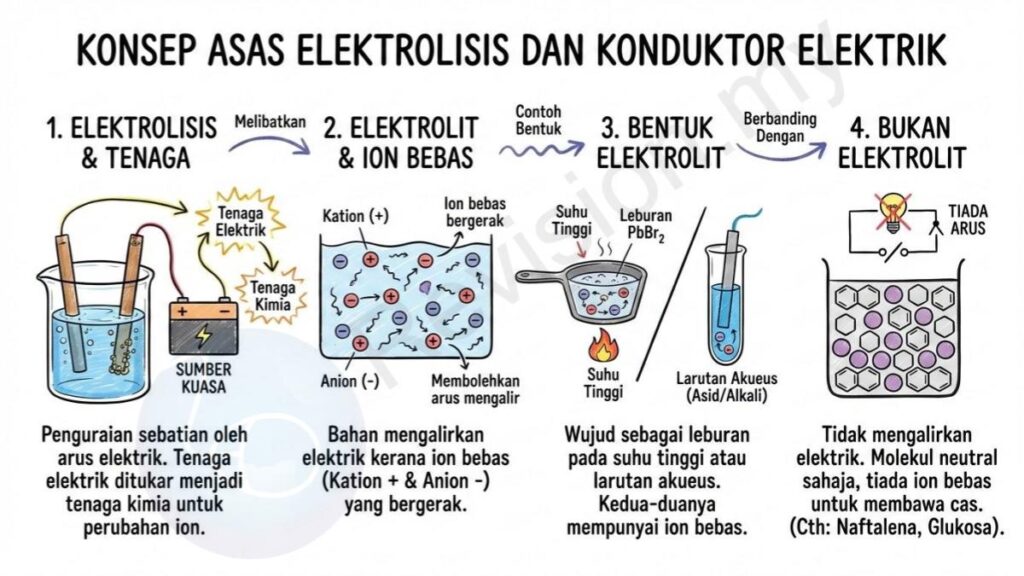
Definisi Elektrolisis: Elektrolisis ialah proses penguraian sebatian apabila arus elektrik mengalir melaluinya. Ini bermaksud suatu bahan dipecahkan kepada komponen lebih ringkas dengan bantuan tenaga elektrik yang memaksa tindak balas berlaku walaupun tindak balas itu tidak spontan.
Penukaran Tenaga: Dalam proses elektrolisis, tenaga elektrik daripada sumber kuasa ditukar kepada tenaga kimia. Ini berlaku apabila ion dalam bahan berubah menjadi bentuk baharu, sama ada menjadi logam, gas, atau bahan lain di elektrod.
Elektrolit: Elektrolit ialah bahan yang boleh mengalirkan elektrik kerana ia mempunyai ion bebas yang bergerak. Ketika elektrolisis berlaku, bahan ini juga mengalami perubahan kimia kerana ion-ionnya terlibat secara langsung dalam tindak balas.
Ion dalam Elektrolit: Elektrolit terdiri daripada dua jenis ion, iaitu kation (ion bercas positif) dan anion (ion bercas negatif). Ion-ion ini bebas bergerak dalam leburan atau larutan, dan pergerakan bebas inilah yang membolehkan arus elektrik mengalir.
Bentuk Elektrolit: Elektrolit boleh wujud sama ada sebagai leburan pada suhu tinggi seperti PbBr₂ leburan atau sebagai larutan akueus seperti asid dan alkali. Kedua-dua bentuk ini mempunyai ion bebas yang boleh bergerak.
Bukan Elektrolit: Bahan bukan elektrolit tidak dapat mengalirkan elektrik kerana ia tidak mempunyai ion bebas. Bahan ini hanya terdiri daripada molekul neutral yang tidak boleh membawa cas elektrik.
Contoh Bukan Elektrolit: Naftalena, benzena, larutan glukosa dan sebatian kovalen lain adalah contoh bukan elektrolit. Semua bahan ini tidak menghasilkan ion dalam keadaan biasa dan oleh itu gagal mengalirkan elektrik.
Proses Elektrolisis dan Terminal
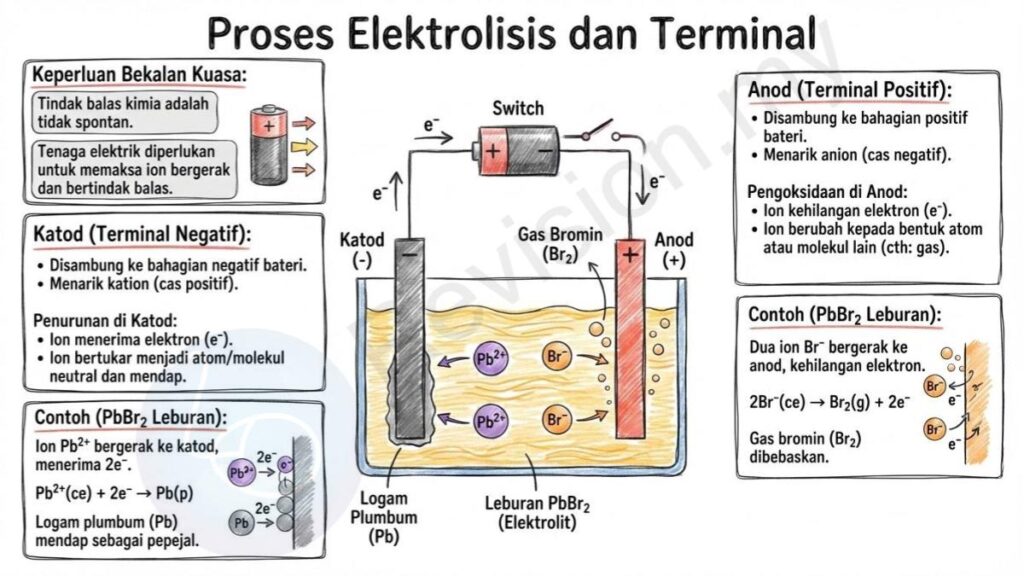
Keperluan Bekalan Kuasa: Elektrolisis memerlukan bekalan tenaga elektrik daripada sumber seperti bateri kerana tindak balas kimia yang berlaku adalah tidak spontan. Ini bermaksud tindak balas hanya boleh berlaku apabila tenaga elektrik dibekalkan untuk memaksa ion bergerak dan bertindak balas.
Katod (Terminal Negatif): Katod ialah terminal negatif yang disambungkan kepada bahagian negatif bateri. Terminal ini akan menarik kation kerana kation mempunyai cas positif yang tertarik kepada cas negatif pada katod.
Penurunan di Katod: Di katod, proses penurunan berlaku apabila ion menerima elektron yang mengalir dari bateri melalui wayar. Apabila ion menerima elektron, ia bertukar menjadi atom atau molekul neutral dan mendap pada elektrod.
Contoh di Katod: Contohnya, dalam elektrolisis PbBr₂ leburan, ion plumbum Pb²⁺ bergerak ke arah katod dan menerima dua elektron. Proses ini menyebabkan Pb²⁺ bertukar menjadi logam plumbum, Pb, yang mendap sebagai pepejal.
Anod (Terminal Positif): Anod ialah terminal positif yang disambungkan kepada bahagian positif bateri. Anod menarik anion kerana anion mempunyai cas negatif yang tertarik kepada cas positif pada anod.
Pengoksidaan di Anod: Di anod, proses pengoksidaan berlaku apabila ion kehilangan elektron. Kehilangan elektron ini menyebabkan ion berubah kepada bentuk atom atau molekul lain seperti gas.
Contoh di Anod: Sebagai contoh, dalam elektrolisis PbBr₂ leburan, dua ion Br⁻ bergerak ke anod dan kehilangan elektron. Kehilangan dua elektron ini menyebabkan ion Br⁻ bertukar menjadi gas bromin, Br₂, yang dibebaskan di anod.
Faktor yang Mempengaruhi Hasil Elektrolisis Larutan Akueus
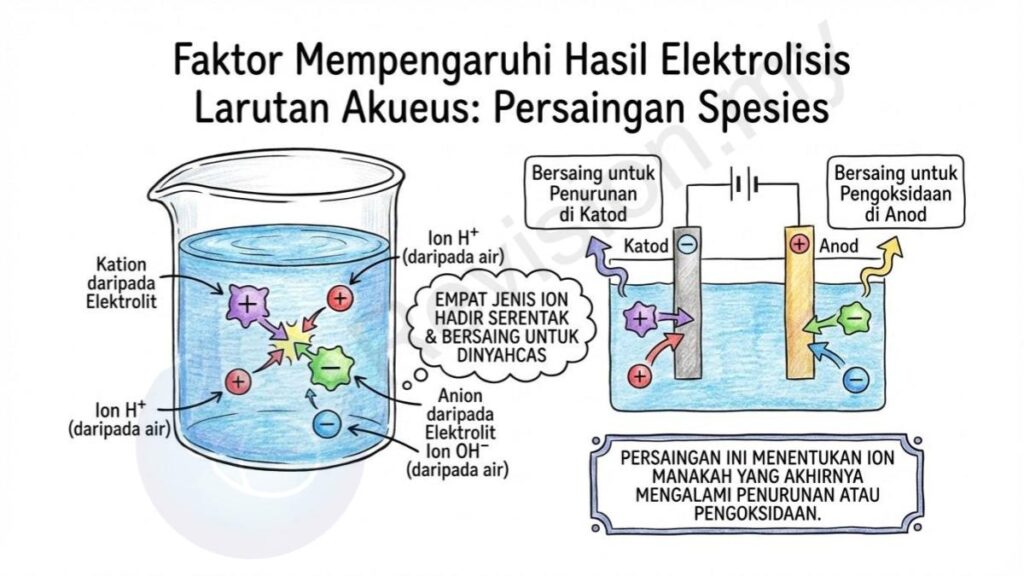
Persaingan Spesies: Dalam larutan akueus, terdapat empat jenis ion yang hadir serentak, dan semuanya akan bersaing untuk dinyahcas di elektrod. Ion-ion tersebut ialah kation daripada elektrolit, ion H⁺ yang berasal daripada air, anion daripada elektrolit, serta ion OH⁻ yang juga datang daripada air. Persaingan ini menentukan ion manakah yang akhirnya mengalami penurunan atau pengoksidaan.
Nilai E° / Siri Elektrokimia (SEK)
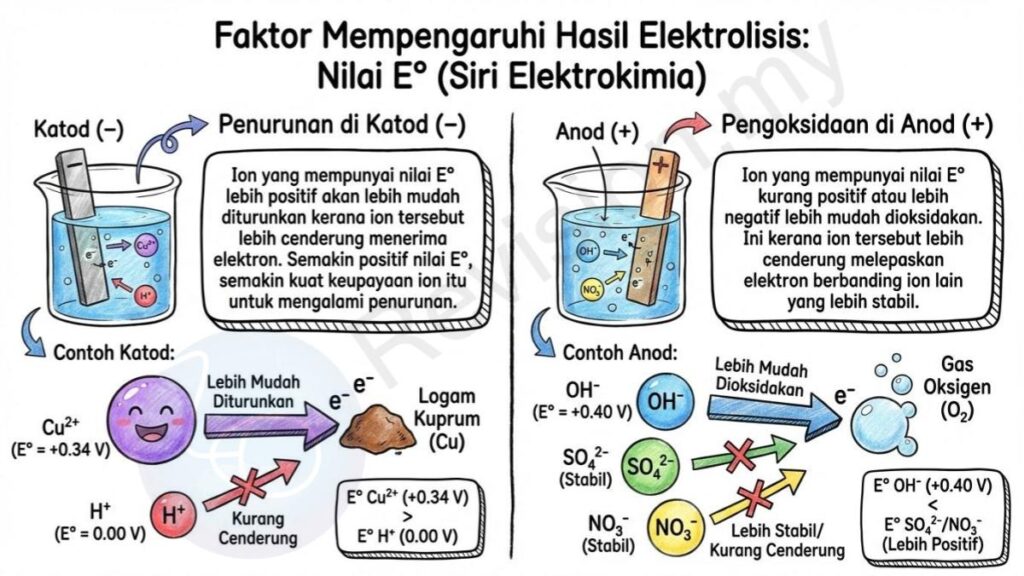
Penurunan di Katod: Ion yang mempunyai nilai E° lebih positif akan lebih mudah diturunkan kerana ion tersebut lebih cenderung menerima elektron. Semakin positif nilai E°, semakin kuat keupayaan ion itu untuk mengalami penurunan.
Contoh Katod: Sebagai contoh, ion Cu²⁺ dengan nilai E° = +0.34 V lebih mudah diturunkan berbanding ion H⁺ yang mempunyai nilai E° = 0.00 V. Ini menunjukkan bahawa Cu²⁺ lebih berkemampuan menerima elektron.
Pengoksidaan di Anod: Ion yang mempunyai nilai E° kurang positif atau lebih negatif lebih mudah dioksidakan. Ini kerana ion tersebut lebih cenderung melepaskan elektron berbanding ion lain yang lebih stabil.
Contoh Anod: Sebagai contoh, OH⁻ lebih mudah dioksidakan kerana E° = +0.40 V, manakala ion SO₄²⁻ dan NO₃⁻ adalah lebih stabil dan tidak mudah melepaskan elektron.
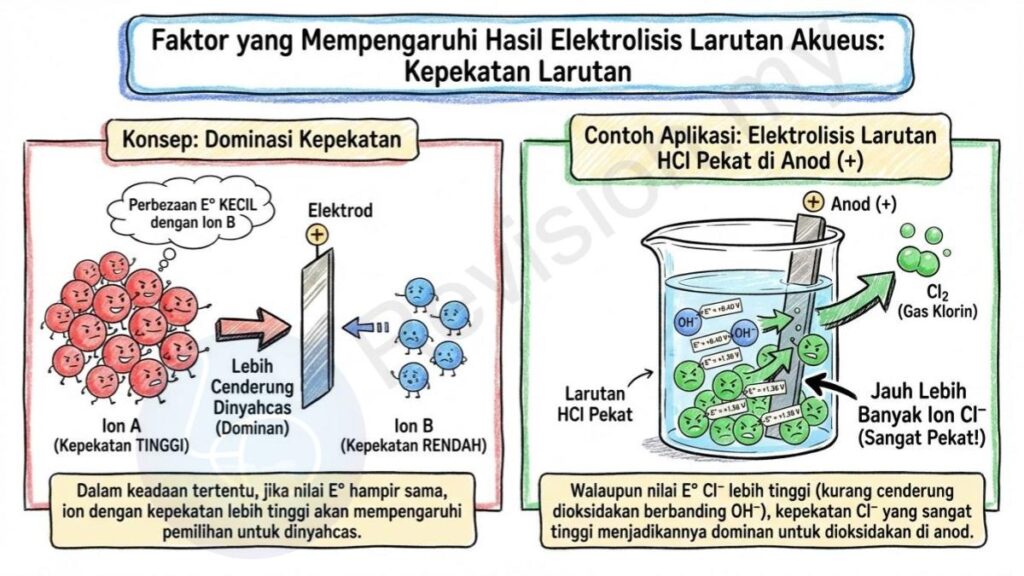
Kepekatan Larutan
Dominasi Kepekatan: Dalam keadaan tertentu, jika perbezaan nilai E° antara dua ion adalah sangat kecil, kepekatan ion yang lebih tinggi boleh mempengaruhi pemilihan ion yang dinyahcas di elektrod.
Contoh Kepekatan: Contohnya, dalam larutan HCl pekat, jumlah ion Cl⁻ adalah sangat tinggi sehingga ia lebih mudah dioksidakan di anod walaupun nilai E° nya lebih tinggi daripada OH⁻. Kepekatan yang tinggi menjadikan Cl⁻ lebih dominan dalam tindak balas.
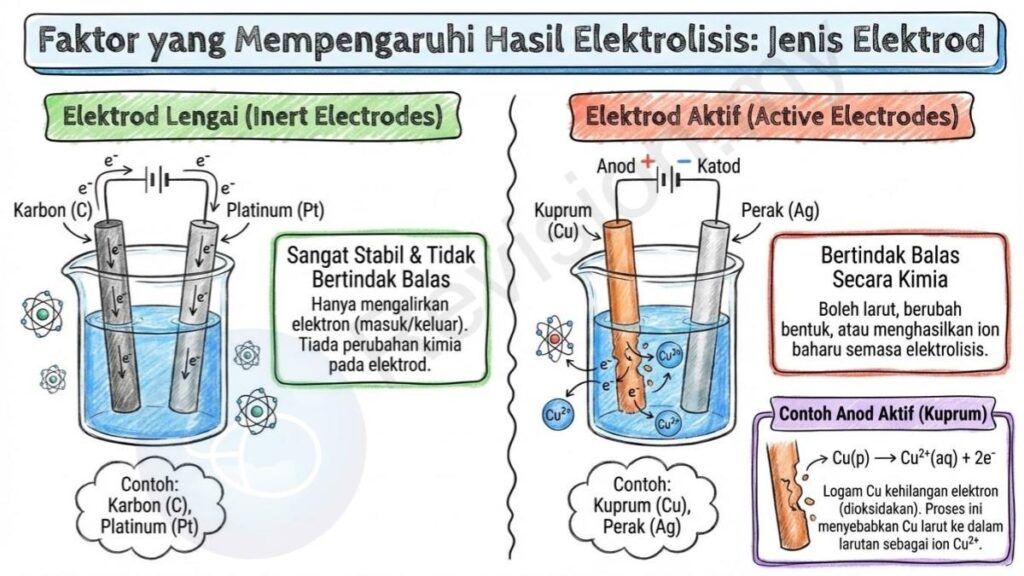
Jenis Elektrod
Elektrod Lengai: Elektrod seperti karbon dan platinum tidak mengambil bahagian dalam tindak balas kimia kerana ia sangat stabil. Peranan utama elektrod ini hanyalah untuk mengalirkan elektron masuk dan keluar daripada sel tanpa mengalami sebarang perubahan kimia.
Elektrod Aktif: Elektrod seperti kuprum (Cu) dan perak (Ag) boleh bertindak balas secara kimia dengan ion dalam larutan. Ini bermaksud elektrod ini boleh larut, berubah bentuk atau menghasilkan ion baharu semasa elektrolisis berlaku.
Contoh Anod Aktif: Dalam elektrolisis yang menggunakan anod kuprum, logam kuprum akan kehilangan elektron dan mengalami pengoksidaan. Proses ini menyebabkan kuprum larut ke dalam larutan sebagai ion Cu²⁺.
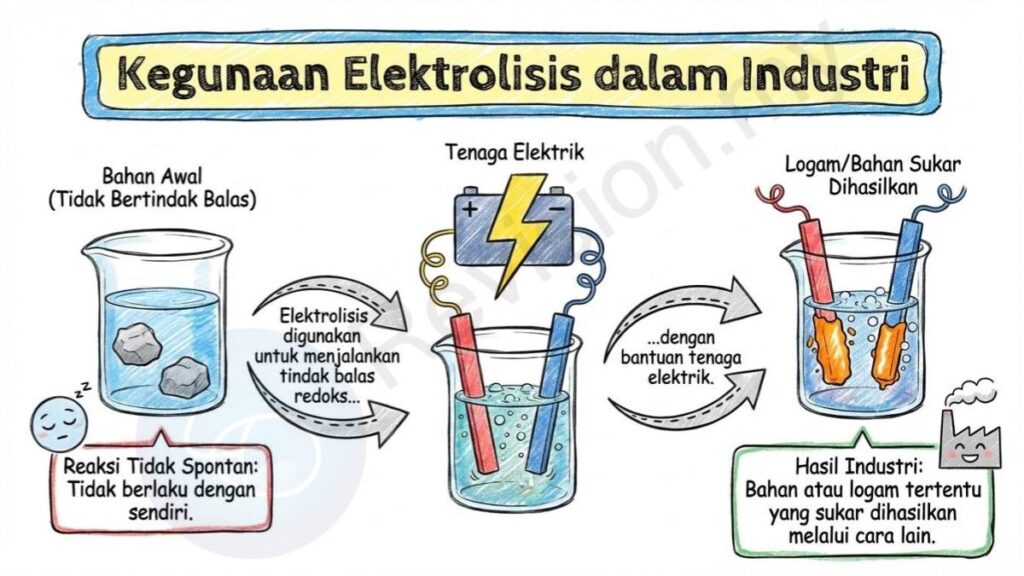
Kegunaan Elektrolisis dalam Industri
Reaksi Tidak Spontan: Elektrolisis digunakan untuk menjalankan tindak balas redoks yang tidak berlaku dengan sendiri. Dengan bantuan tenaga elektrik, industri boleh menghasilkan bahan atau logam tertentu yang sukar dihasilkan melalui cara lain.
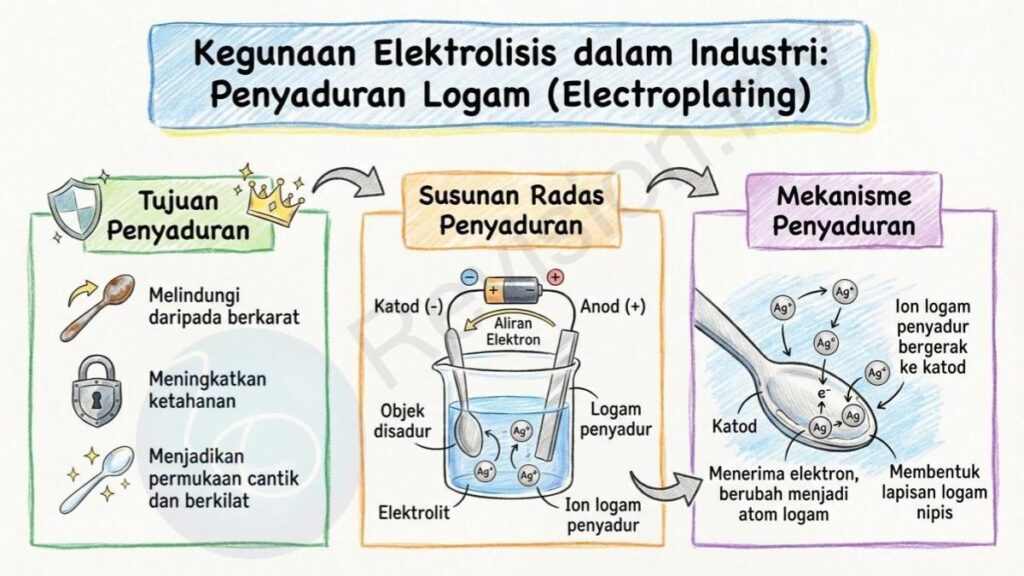
Penyaduran Logam
Tujuan Penyaduran: Penyaduran dilakukan untuk melindungi logam daripada berkarat, meningkatkan ketahanannya, atau menjadikan permukaannya lebih cantik dan berkilat.
Susunan Radas Penyaduran: Dalam proses penyaduran, objek yang ingin disadur disambungkan sebagai katod supaya ia dapat menerima elektron. Logam penyadur pula menjadi anod supaya logam tersebut boleh larut sebagai ion ke dalam elektrolit. Elektrolit yang digunakan mengandungi ion logam penyadur.
Mekanisme Penyaduran: Ion logam penyadur dalam elektrolit akan bergerak menuju ke katod dan menerima elektron. Apabila ia diturunkan, ion tersebut berubah menjadi atom logam dan membentuk satu lapisan logam nipis pada permukaan objek yang disadur.
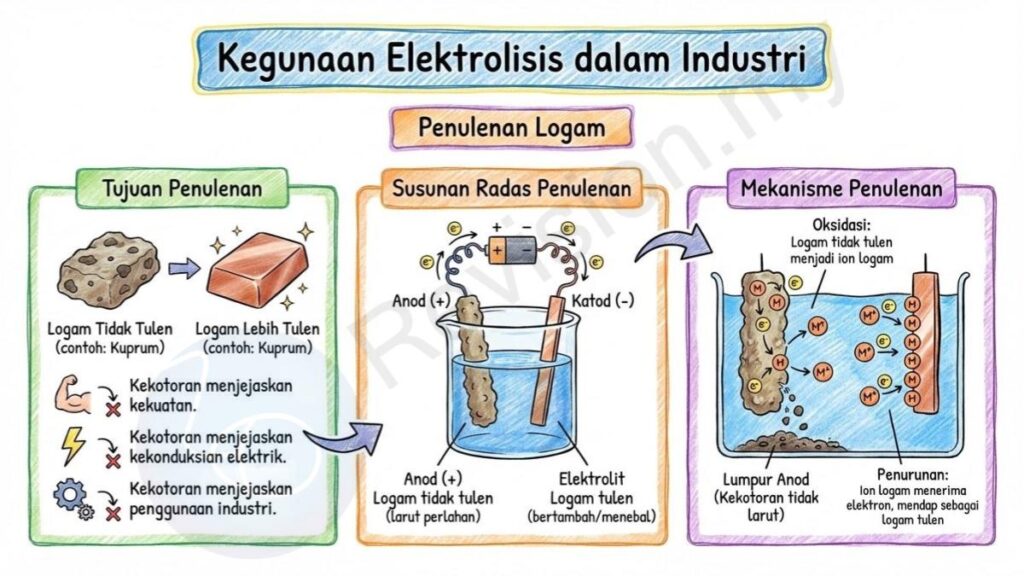
Penulenan Logam
Tujuan Penulenan: Penulenan digunakan untuk mendapatkan logam yang lebih tulen seperti kuprum atau perak daripada logam tidak tulen. Proses ini penting kerana logam yang tidak tulen mengandungi kekotoran yang boleh menjejaskan kekuatannya, kekonduksian elektrik dan penggunaannya dalam industri.
Susunan Radas Penulenan: Dalam proses penulenan logam, anod ialah logam tidak tulen yang akan larut secara perlahan apabila arus elektrik mengalir. Katod pula ialah logam tulen yang akan bertambah kerana ion logam dari anod bergerak dan mendap pada katod.
Mekanisme Penulenan: Logam tidak tulen di anod akan dioksidakan menjadi ion logam dan masuk ke dalam larutan. Ion ini kemudian bergerak menuju ke katod di mana ia menerima elektron dan diturunkan semula menjadi logam tulen. Kekotoran yang tidak larut akan gugur ke dasar sebagai lumpur anod.
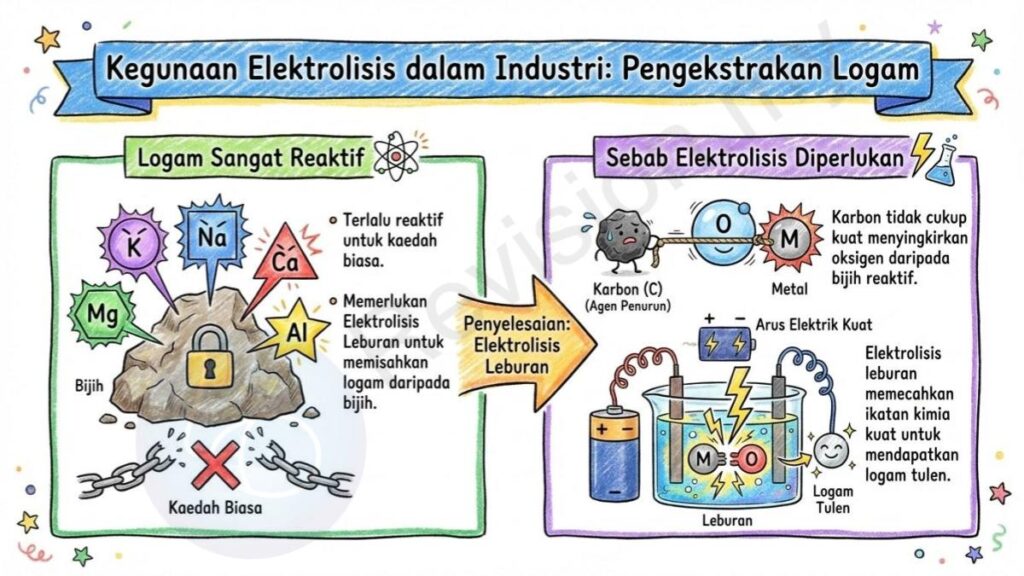
Pengekstrakan Logam
Logam Sangat Reaktif: Logam seperti kalium (K), natrium (Na), kalsium (Ca), magnesium (Mg) dan aluminium (Al) sangat reaktif sehingga logam-logam ini tidak boleh diekstrak menggunakan kaedah biasa. Oleh itu, elektrolisis leburan digunakan untuk memisahkan logam-logam ini daripada bijihnya.
Sebab Elektrolisis: Logam-logam ini terlalu reaktif untuk diekstrak menggunakan karbon sebagai agen penurun kerana karbon tidak cukup kuat untuk menyingkirkan oksigen daripada bijih reaktif tersebut. Oleh sebab itu, elektrolisis leburan diperlukan untuk memecahkan ikatan kimia dan mendapatkan logam tulen.