9.3 Sel Kimia (Sel Voltaik/Galvanik)
Fungsi dan Prinsip Asas
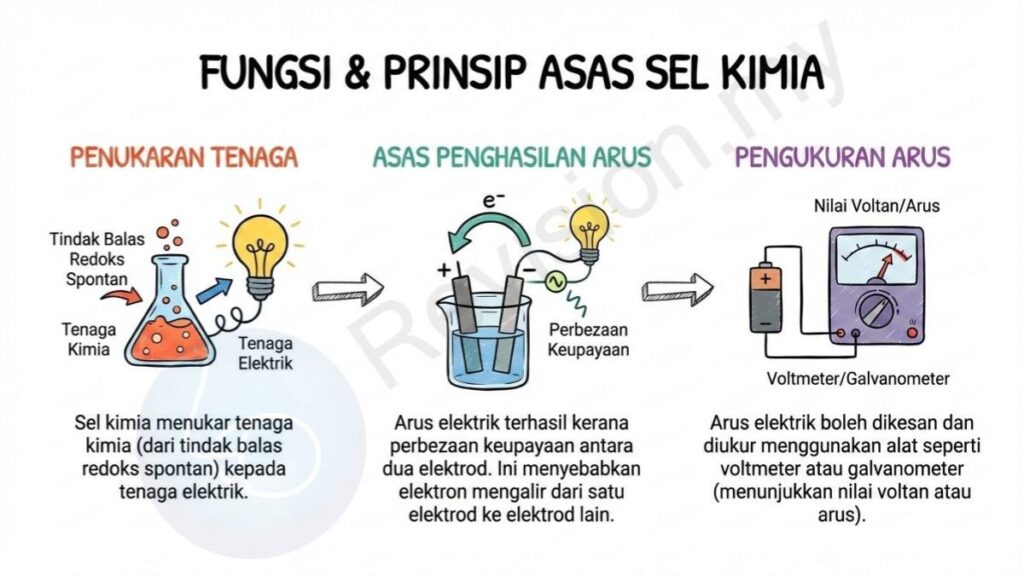
Penukaran Tenaga: Sel kimia menukar tenaga kimia yang tersimpan dalam tindak balas redoks spontan kepada tenaga elektrik. Ini bermakna tindak balas kimia yang berlaku menghasilkan tenaga yang boleh digunakan sebagai arus elektrik.
Asas Penghasilan Arus: Arus elektrik terhasil kerana terdapat perbezaan keupayaan antara dua elektrod dalam sel. Perbezaan ini menyebabkan elektron mengalir dari satu elektrod ke elektrod yang lain.
Pengukuran Arus: Arus elektrik yang dihasilkan oleh sel kimia boleh dikesan dan diukur menggunakan alat seperti voltmeter atau galvanometer untuk menunjukkan nilai voltan atau arus.
Struktur dan Komponen Utama
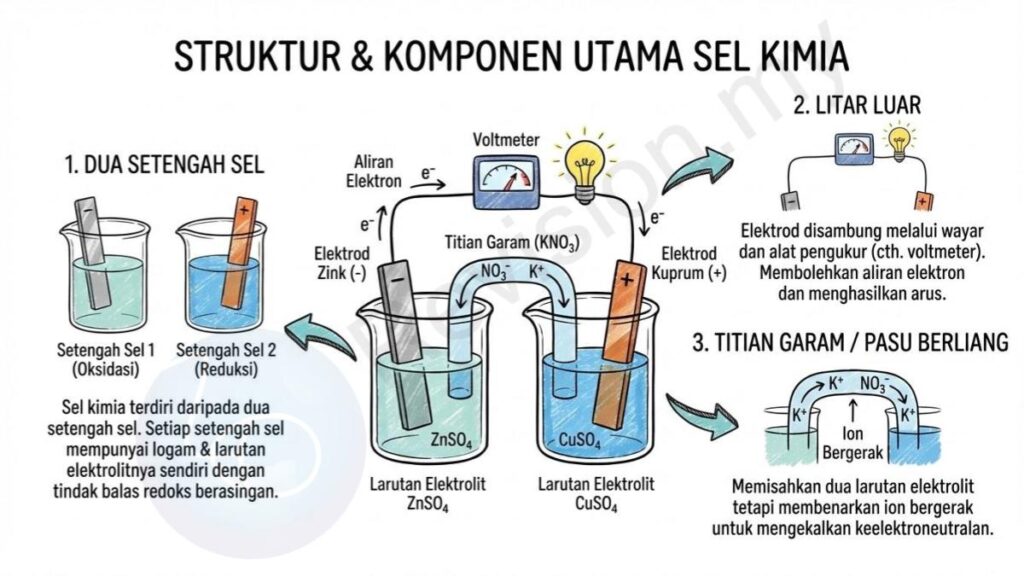
Dua Setengah Sel: Sel kimia terdiri daripada dua setengah sel, iaitu dua logam yang berada dalam larutan elektrolit masing-masing atau kadangkala berkongsi larutan yang sama. Setiap setengah sel mempunyai tindak balas redoksnya sendiri.
Litar Luar: Dua elektrod dalam sel disambungkan menggunakan wayar melalui alat pengukur seperti voltmeter. Sambungan ini membolehkan elektron mengalir antara elektrod dan menghasilkan arus.
Titian Garam / Pasu Berliang: Titian garam atau pasu berliang berfungsi memisahkan dua larutan elektrolit tetapi masih membenarkan ion bergerak antara kedua-duanya. Ini memastikan keelektroneutralan dalam sel dikekalkan ketika tindak balas berlaku.
Terminal Elektrod Berdasarkan E°
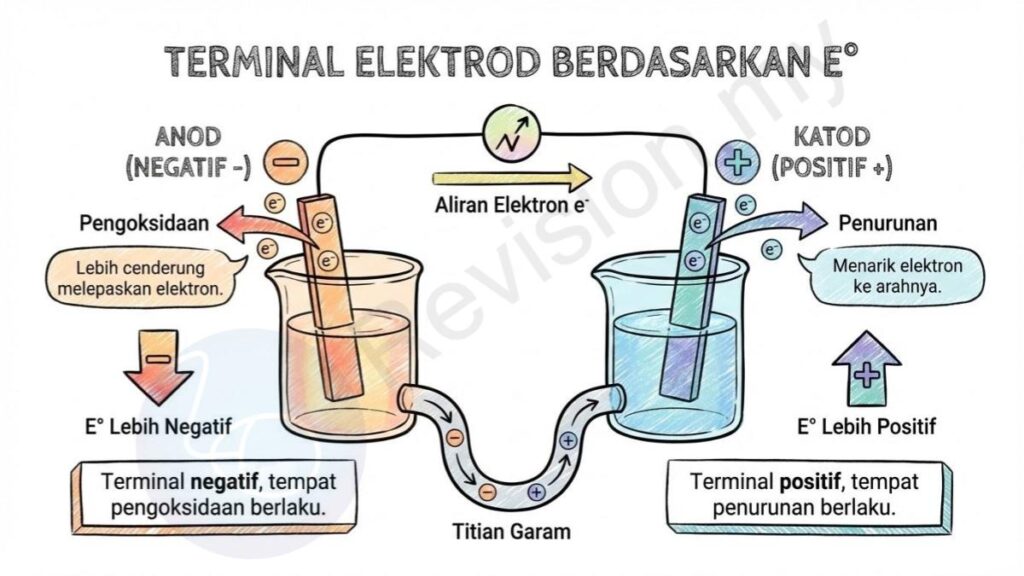
Anod (Negatif): Anod ialah terminal negatif dalam sel kimia di mana tindak balas pengoksidaan berlaku. Ia mempunyai nilai E° yang lebih negatif kerana lebih cenderung melepaskan elektron.
Katod (Positif): Katod ialah terminal positif dalam sel kimia di mana tindak balas penurunan berlaku. Ia mempunyai nilai E° yang lebih positif dan menarik elektron ke arahnya.
Aliran Elektron dan Ion
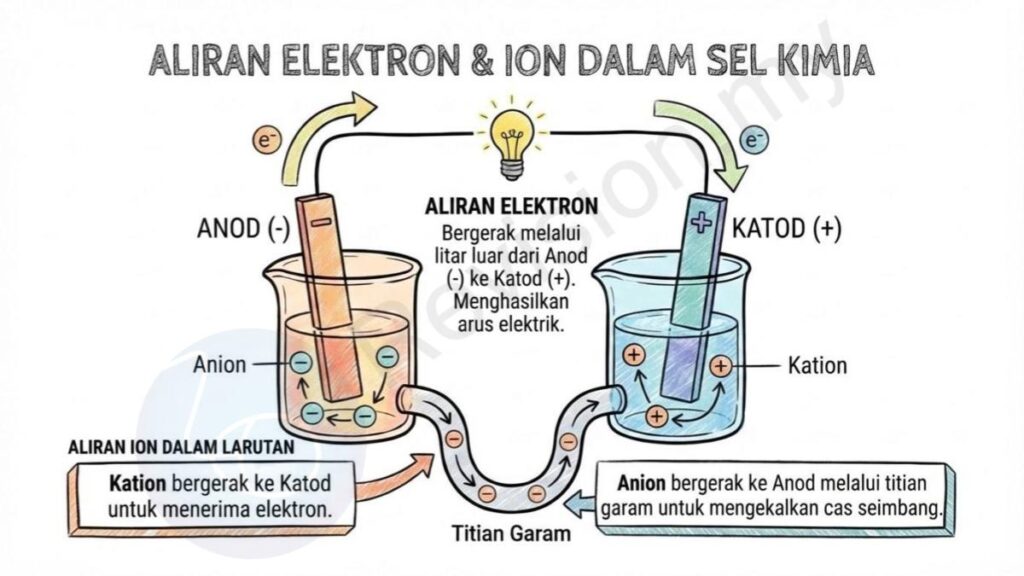
Aliran Elektron: Elektron sentiasa bergerak melalui litar luar dari anod yang bercas negatif ke katod yang bercas positif. Pergerakan ini menghasilkan arus elektrik.
Aliran Ion dalam Larutan: Dalam larutan, kation akan bergerak ke katod untuk menerima elektron, manakala anion bergerak ke anod melalui titian garam untuk mengekalkan cas seimbang.
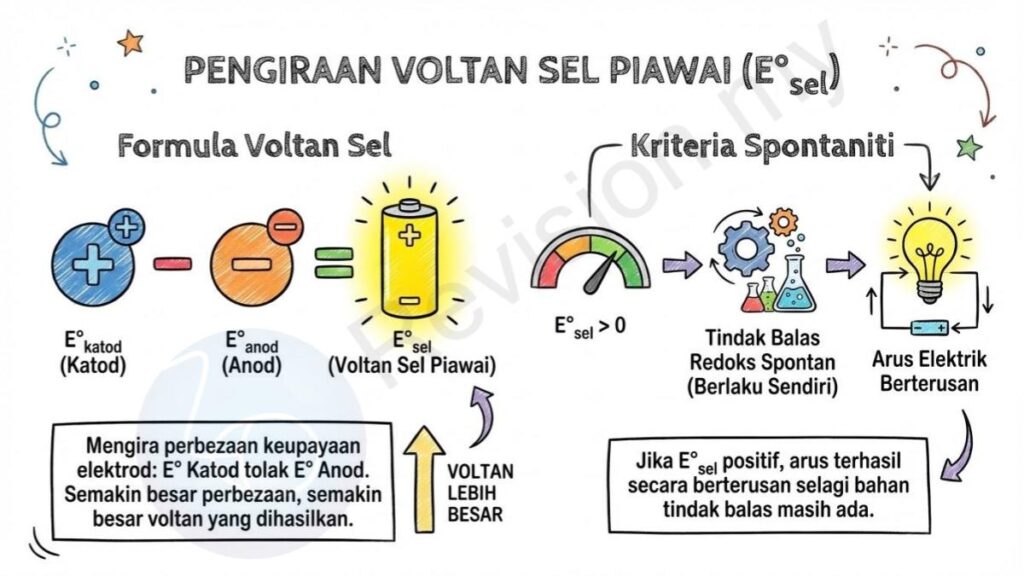
Pengiraan Voltan Sel Piawai (E°ₛₑₗ)
Formula Voltan Sel: Nilai voltan sel piawai boleh dikira menggunakan formula E°ₛₑₗ = E°ₖₐₜₒ𝒹 − E°ₐₙₒ𝒹. Formula ini bermaksud kita mengambil nilai keupayaan elektrod di katod dan menolak nilai keupayaan elektrod di anod untuk melihat perbezaannya. Semakin besar perbezaan ini, semakin besar voltan yang boleh dihasilkan oleh sel.
Kriteria Spontaniti: Jika nilai E°ₛₑₗ lebih besar daripada sifar, ini menunjukkan tindak balas redoks berlaku dengan sendiri tanpa memerlukan tenaga tambahan. Oleh itu, arus elektrik boleh terhasil secara berterusan selagi bahan tindak balas masih ada.
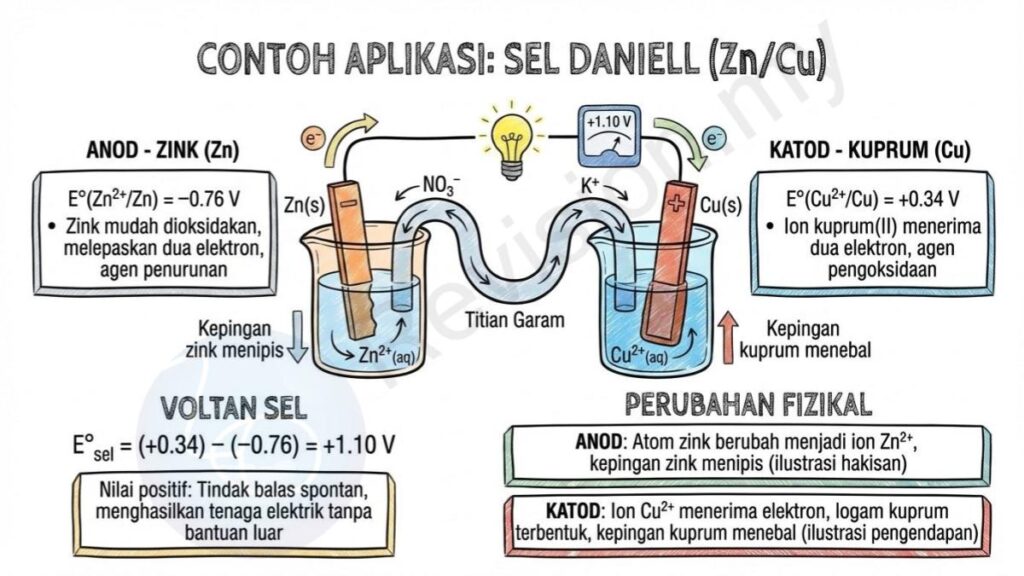
Contoh Aplikasi: Sel Daniell (Zn/Cu)
Anod – Zink (Zn):
- E°(Zn²⁺/Zn) = −0.76 V. • Zink mudah dioksidakan kerana ia melepaskan dua elektron dengan cepat, menjadikannya agen penurunan kerana ia menyumbangkan elektron kepada bahan lain.
- Setengah persamaan: Zn(s) → Zn²⁺(aq) + 2e⁻. Persamaan ini menunjukkan zink berubah daripada logam kepada ion sambil melepaskan dua elektron.
Katod – Kuprum (Cu):
- E°(Cu²⁺/Cu) = +0.34 V.
- Ion kuprum(II) menerima dua elektron dan bertindak sebagai agen pengoksidaan kerana ia mengambil elektron daripada zink dalam tindak balas.
- Setengah persamaan: Cu²⁺(aq) + 2e⁻ → Cu(s). Ini menunjukkan ion kuprum bertukar menjadi logam kuprum selepas menerima elektron.
Voltan Sel: E°ₛₑₗ = (+0.34) − (−0.76) = +1.10 V. Nilai positif ini membuktikan bahawa tindak balas berlaku secara spontan dan boleh menghasilkan tenaga elektrik tanpa bantuan luar.
Perubahan Fizikal: Kepingan zink semakin menipis dari masa ke masa kerana atom zink berubah menjadi ion Zn²⁺ dan larut dalam larutan. Dalam masa yang sama, logam kuprum terbentuk pada elektrod kuprum apabila ion Cu²⁺ menerima elektron, menyebabkan kepingan kuprum menjadi semakin tebal.