9.1 Pengoksidaan dan Pengurangan
Tindak Balas Redoks
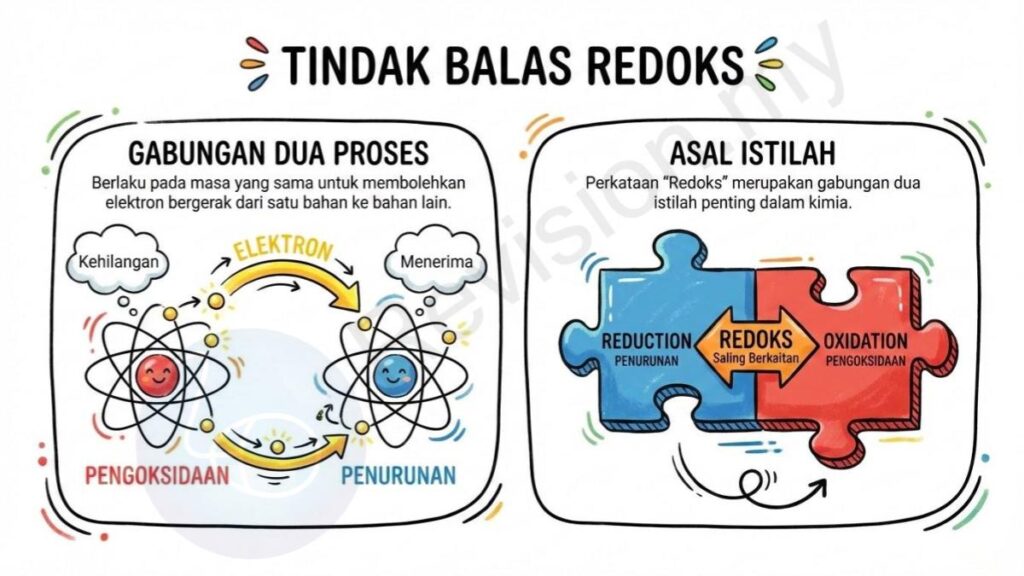
Gabungan Dua Proses: Tindak balas redoks melibatkan dua proses yang berlaku pada masa yang sama, iaitu pengoksidaan dan penurunan, dan kedua-duanya mesti berlaku bersama supaya elektron dapat bergerak dari satu bahan ke bahan lain.
Asal Istilah: Perkataan ‘Redoks’ merupakan gabungan dua istilah penting dalam kimia, iaitu ‘Reduction’ yang bermaksud penurunan dan ‘Oxidation’ yang bermaksud pengoksidaan, menunjukkan bahawa kedua-dua proses ini saling berkaitan.
Definisi Pengoksidaan dan Penurunan (Mengikut Tiga Kriteria)
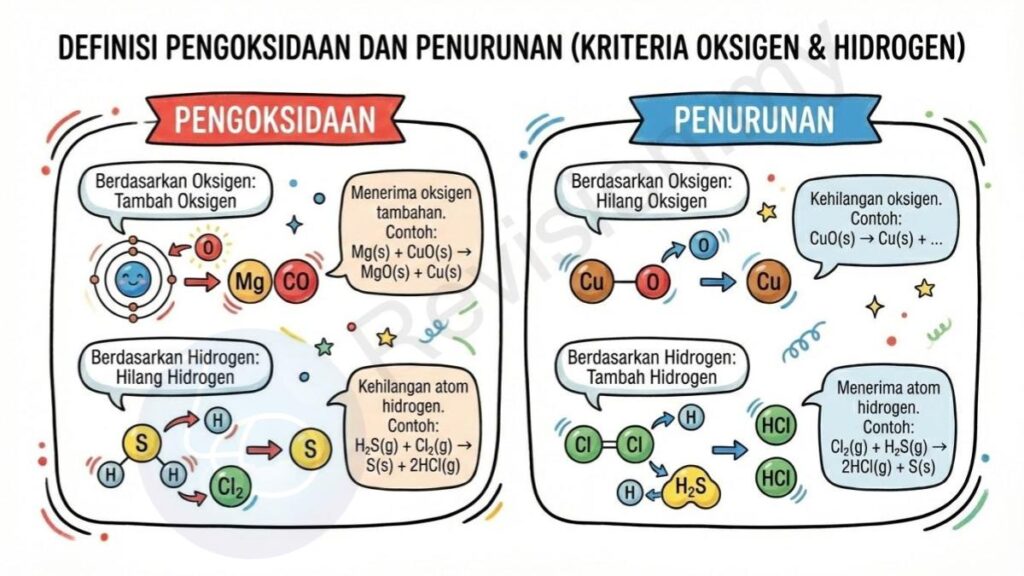
Berdasarkan Oksigen dan Hidrogen
Pengoksidaan – Tambah Oksigen: Pengoksidaan berlaku apabila sesuatu bahan menerima oksigen tambahan, menyebabkan bahan itu menjadi lebih teroksida. Contohnya, dalam tindak balas Mg(s) + CuO(s) → MgO(s) + Cu(s), magnesium menyerap oksigen daripada kuprum oksida.
Pengoksidaan – Hilang Hidrogen: Pengoksidaan juga berlaku apabila suatu bahan kehilangan atom hidrogen yang terikat padanya. Sebagai contoh, dalam tindak balas H₂S(g) + Cl₂(g) → S(s) + 2HCl(g), gas hidrogen sulfida kehilangan hidrogen dan berubah menjadi sulfur.
Penurunan – Hilang Oksigen: Penurunan berlaku apabila bahan kehilangan oksigen, menjadikannya kurang teroksida. Contohnya, kuprum(II) oksida CuO(s) kehilangan oksigen dan bertukar menjadi logam kuprum.
Penurunan – Tambah Hidrogen: Penurunan juga berlaku apabila bahan menerima atom hidrogen. Sebagai contoh, dalam tindak balas dengan H₂S, molekul Cl₂(g) menerima hidrogen untuk membentuk HCl.
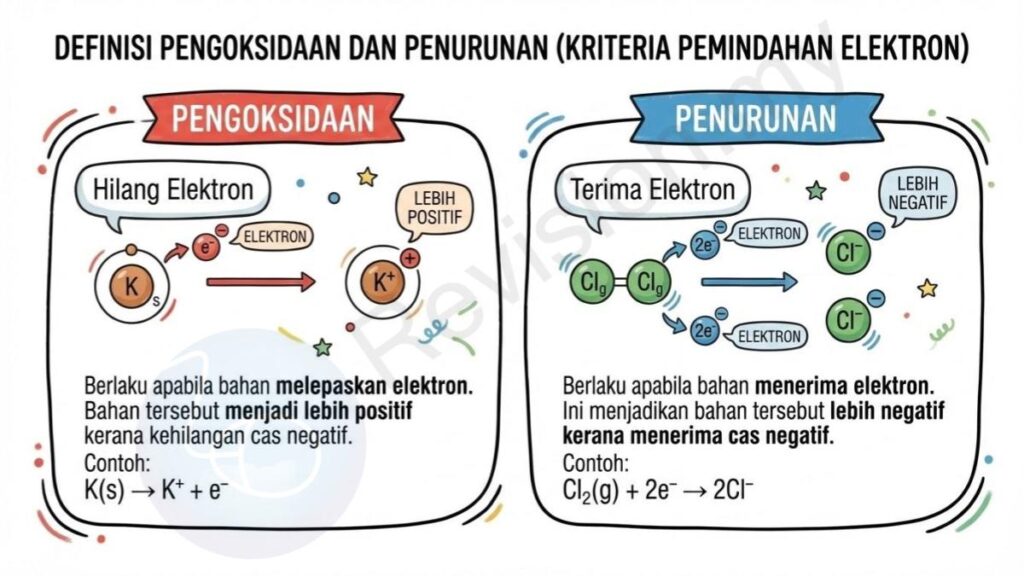
Berdasarkan Pemindahan Elektron
Pengoksidaan – Hilang Elektron: Pengoksidaan berlaku apabila bahan melepaskan elektron. Bahan tersebut menjadi lebih positif kerana kehilangan cas negatif, seperti dalam tindak balas K(s) → K⁺ + e⁻.
Penurunan – Terima Elektron: Penurunan berlaku apabila bahan menerima elektron. Ini menjadikan bahan tersebut lebih negatif kerana menerima cas negatif, contohnya dalam tindak balas Cl₂(g) + 2e⁻ → 2Cl⁻.
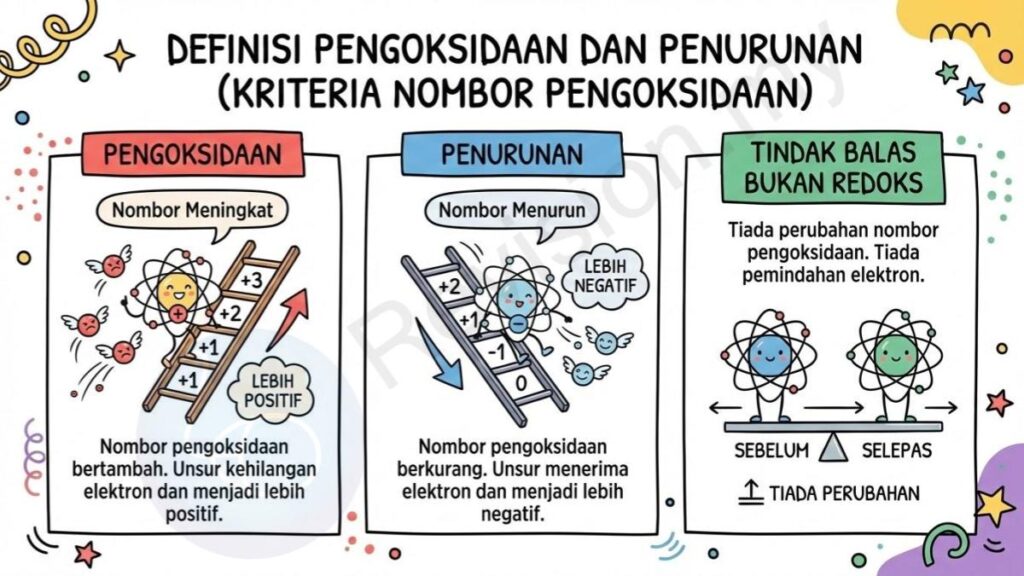
Berdasarkan Nombor Pengoksidaan
Pengoksidaan – Nombor Meningkat: Pengoksidaan berlaku apabila nombor pengoksidaan sesuatu unsur bertambah selepas tindak balas, menunjukkan bahawa unsur tersebut telah kehilangan elektron dan menjadi lebih positif.
Penurunan – Nombor Menurun: Penurunan berlaku apabila nombor pengoksidaan sesuatu unsur berkurang selepas tindak balas, kerana unsur itu telah menerima elektron dan menjadi lebih negatif.
Tindak Balas Bukan Redoks: Tindak balas bukan redoks ialah tindak balas kimia di mana tiada perubahan nombor pengoksidaan berlaku pada mana-mana unsur, menandakan tiada pemindahan elektron.
Agen Pengoksidaan dan Agen Penurunan
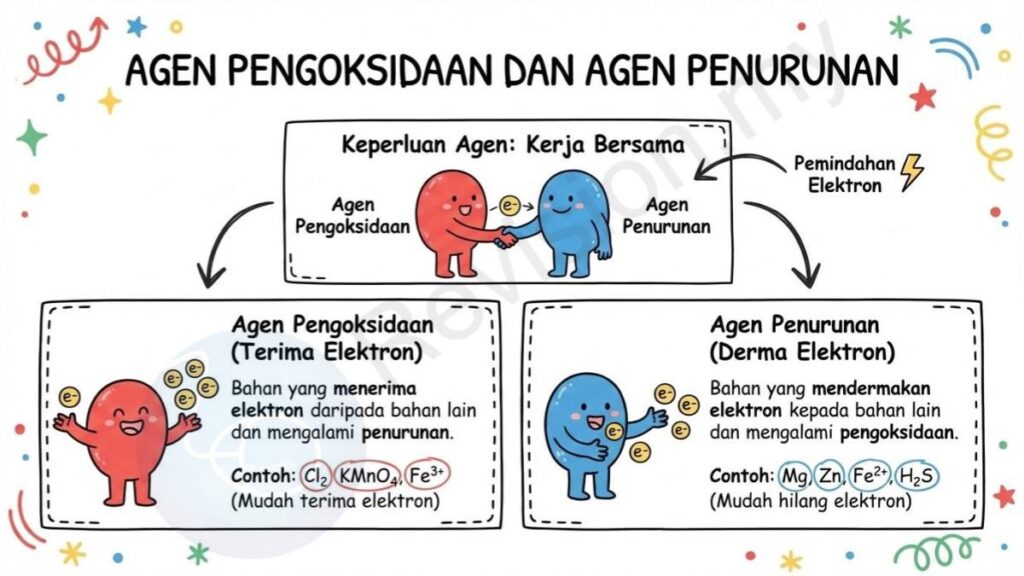
Keperluan Agen: Dalam setiap tindak balas redoks, mesti ada dua agen yang bekerja bersama—satu bertindak sebagai agen pengoksidaan dan satu lagi sebagai agen penurunan, supaya pemindahan elektron dapat berlaku.
Agen Pengoksidaan: Agen pengoksidaan ialah bahan yang menerima elektron daripada bahan lain dan mengalami penurunan. Contohnya termasuk Cl₂, KMnO₄ dan Fe³⁺ yang semuanya mudah menerima elektron.
Agen Penurunan: Agen penurunan ialah bahan yang mendermakan elektron kepada bahan lain dan mengalami pengoksidaan. Antara contoh biasa ialah Mg, Zn, Fe²⁺ dan H₂S yang semuanya mudah kehilangan elektron.
Peraturan Penentuan Nombor Pengoksidaan
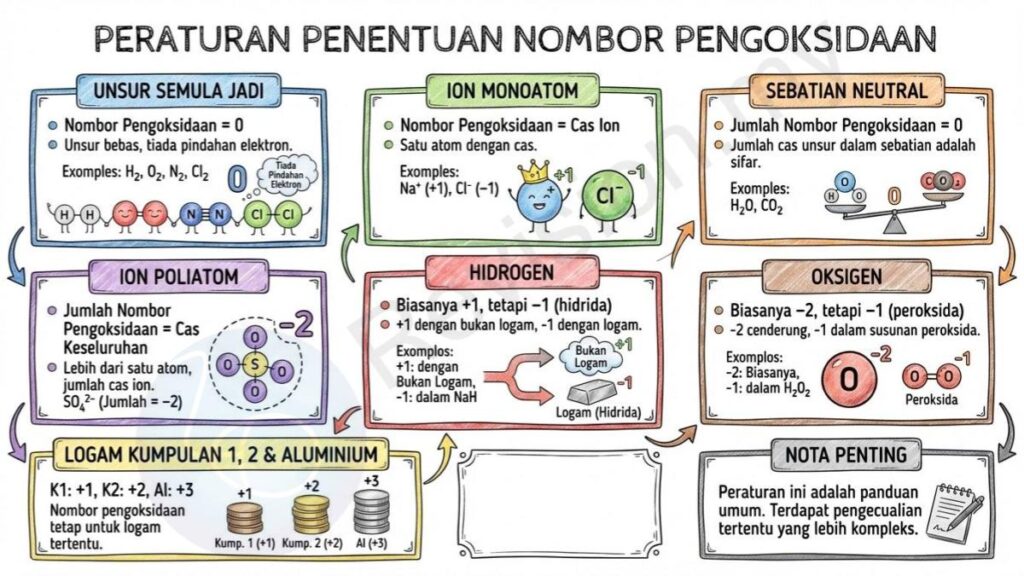
Unsur Semula Jadi: Unsur bebas yang wujud dalam keadaan semula jadi tanpa bergabung dengan unsur lain mempunyai nombor pengoksidaan sifar kerana ia tidak memindahkan atau menerima elektron. Contohnya termasuk H₂, O₂, N₂ dan Cl₂ yang semuanya berada dalam bentuk molekul stabil.
Ion Monoatom: Bagi ion yang terdiri daripada satu atom sahaja, nombor pengoksidaannya adalah sama dengan cas yang dimilikinya. Sebagai contoh, ion natrium Na⁺ mempunyai nombor pengoksidaan +1 manakala ion klorida Cl⁻ mempunyai nombor pengoksidaan −1.
Sebatian Neutral: Dalam sesuatu sebatian yang tidak bercas, jumlah keseluruhan nombor pengoksidaan semua unsur di dalamnya mestilah sama dengan sifar. Sebagai contoh, dalam H₂O dan CO₂, nilai nombor pengoksidaan setiap unsur digabungkan untuk menghasilkan jumlah sifar.
Ion Poliatom: Untuk ion yang terdiri daripada lebih daripada satu atom, jumlah nombor pengoksidaan setiap atom mestilah sama dengan cas keseluruhan ion tersebut. Contohnya, dalam SO₄²⁻, jumlah nombor pengoksidaan semua atom ialah −2.
Hidrogen: Hidrogen biasanya mempunyai nombor pengoksidaan +1 apabila bergabung dengan unsur bukan logam, tetapi nilainya menjadi −1 apabila ia bergabung dengan logam dalam sebatian hidrida seperti NaH.
Oksigen: Oksigen biasanya mempunyai nombor pengoksidaan −2 kerana ia cenderung menerima dua elektron, tetapi dalam peroksida seperti H₂O₂, oksigen mempunyai nombor pengoksidaan −1 disebabkan susunan ikatannya yang berbeza.
Logam Kumpulan 1 & 2: Logam dalam Kumpulan 1 sentiasa mempunyai nombor pengoksidaan +1 manakala logam dalam Kumpulan 2 sentiasa mempunyai nombor pengoksidaan +2. Aluminium pula lazimnya mempunyai nombor pengoksidaan +3 dalam hampir semua sebatian kerana kestabilan elektron luarnya.
Penukaran Antara Fe²⁺ dan Fe³⁺
Fe²⁺ kepada Fe³⁺ (Pengoksidaan)
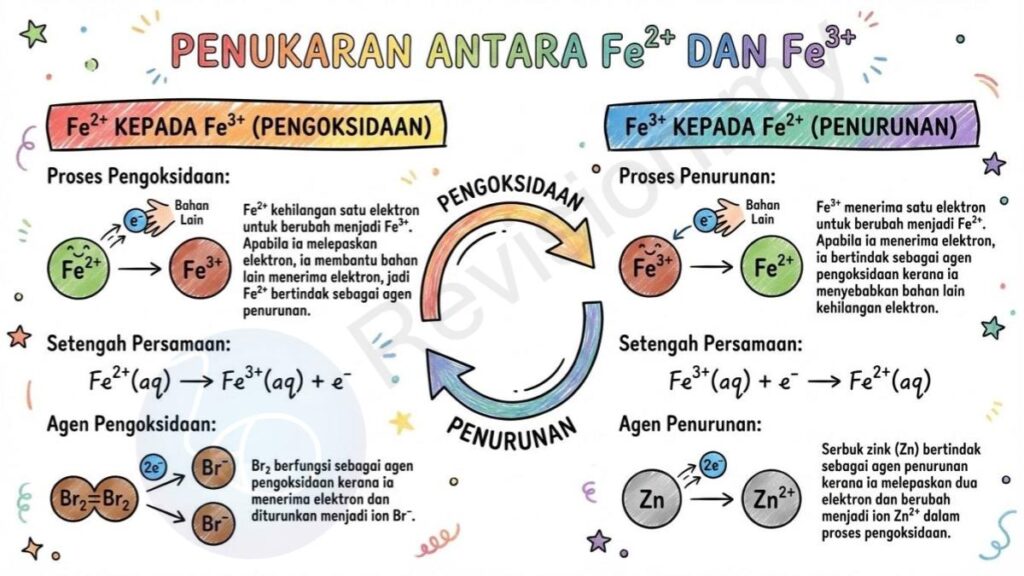
Proses Pengoksidaan: Fe²⁺ kehilangan satu elektron untuk berubah menjadi Fe³⁺. Apabila ia melepaskan elektron, ia sebenarnya membantu bahan lain menerima elektron, jadi Fe²⁺ bertindak sebagai agen penurunan dalam tindak balas ini.
Setengah Persamaan: Fe²⁺(aq) → Fe³⁺(aq) + e⁻. Persamaan ini menunjukkan dengan jelas bagaimana ion Fe²⁺ melepaskan satu elektron semasa proses pengoksidaan.
Agen Pengoksidaan: Br₂ pula berfungsi sebagai agen pengoksidaan kerana ia menerima elektron dan diturunkan menjadi ion Br⁻.
Fe³⁺ kepada Fe²⁺ (Penurunan)
Proses Penurunan: Fe³⁺ menerima satu elektron untuk berubah menjadi Fe²⁺. Apabila ia menerima elektron, ia bertindak sebagai agen pengoksidaan kerana ia menyebabkan bahan lain kehilangan elektron.
Setengah Persamaan: Fe³⁺(aq) + e⁻ → Fe²⁺(aq). Persamaan ini menunjukkan dengan jelas bagaimana Fe³⁺ memperoleh elektron semasa proses penurunan.
Agen Penurunan: Serbuk zink (Zn) bertindak sebagai agen penurunan kerana ia melepaskan dua elektron dan berubah menjadi ion Zn²⁺ dalam proses pengoksidaan.
Tindak Balas Penyesaran Logam daripada Larutan Garam
Prinsip Elektropositiviti dan Spontaniti
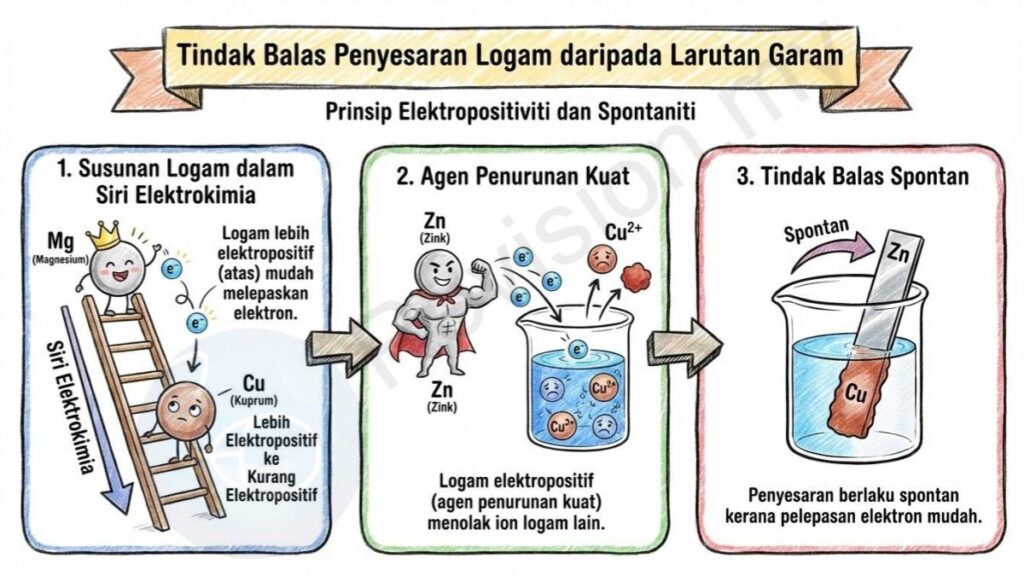
Susunan Logam: Logam yang lebih elektropositif berada di bahagian atas dalam Siri Elektrokimia kerana ia lebih mudah melepaskan elektron berbanding logam lain yang berada di bawahnya.
Agen Penurunan Kuat: Logam elektropositif sangat mudah melepaskan elektron, menjadikannya agen penurunan yang kuat kerana ia boleh menolak ion logam lain daripada larutannya.
Tindak Balas Spontan: Tindak balas berlaku secara spontan apabila logam yang lebih elektropositif menyesarkan ion logam yang kurang elektropositif daripada larutannya kerana pelepasan elektron mudah berlaku.
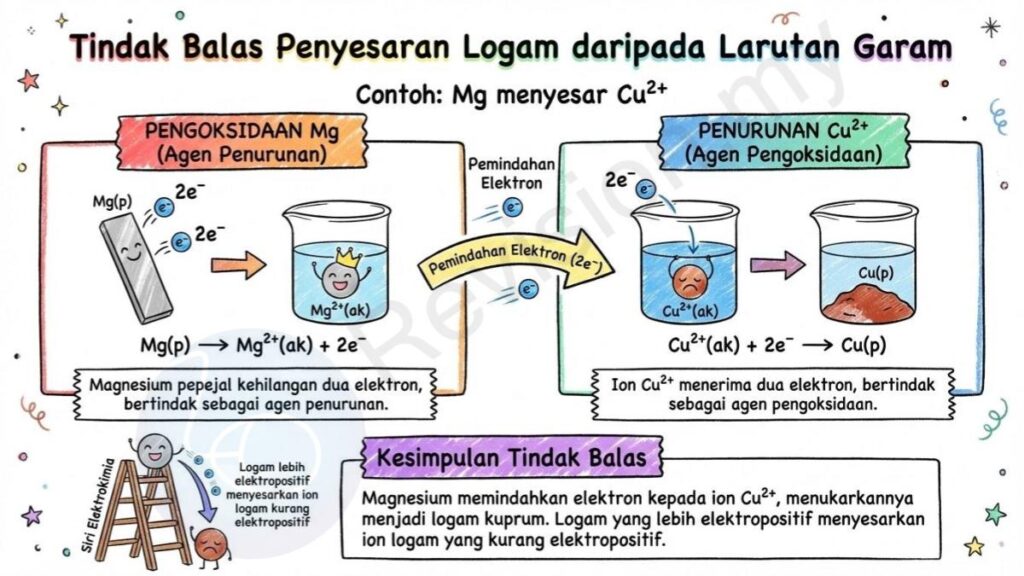
Contoh: Mg menyesar Cu²⁺
Pengoksidaan Mg: Dalam tindak balas ini, magnesium pepejal kehilangan dua elektron lalu berubah menjadi ion Mg²⁺, menjadikannya bertindak sebagai agen penurunan kerana ia mendermakan elektron.
Penurunan Cu²⁺: Ion Cu²⁺ dalam larutan menerima dua elektron lalu bertukar menjadi logam kuprum, menyebabkan ia bertindak sebagai agen pengoksidaan kerana ia menerima elektron daripada magnesium.
Kesimpulan Tindak Balas: Secara keseluruhan, magnesium memindahkan elektron kepada ion Cu²⁺ sehingga menukarkannya menjadi logam kuprum, menunjukkan logam yang lebih elektropositif mampu menyesarkan ion logam yang kurang elektropositif.
Tindak Balas Penyesaran Halogen daripada Larutan Halida
Prinsip Keelektronegatifan dan Agen Pengoksidaan
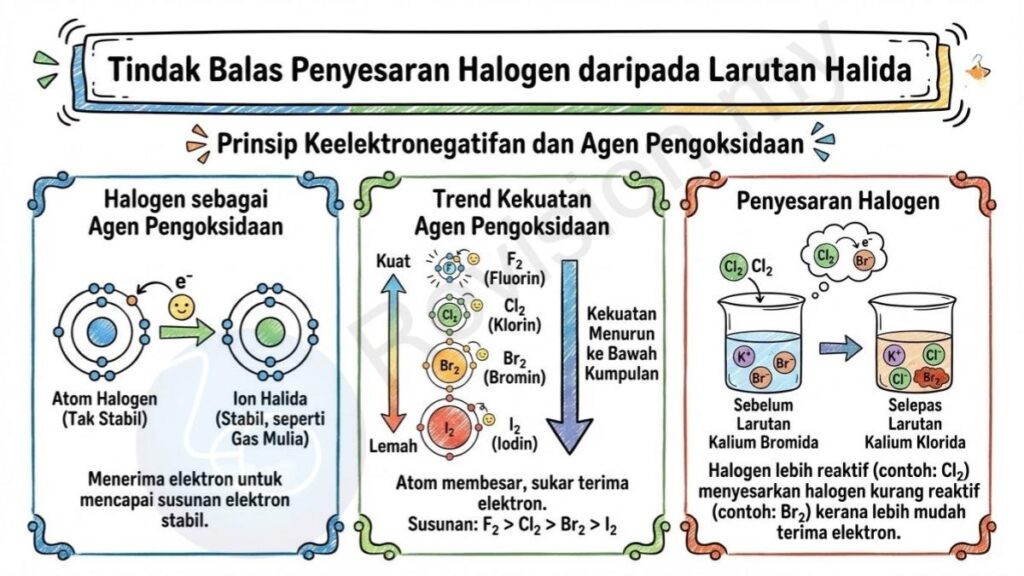
Halogen sebagai Agen Pengoksidaan: Halogen menerima elektron untuk mencapai susunan elektron yang lebih stabil seperti gas mulia. Ini bermaksud setiap atom halogen cuba melengkapkan bilangan elektron dalam petala terluarnya supaya ia menjadi lebih stabil.
Trend Kekuatan Agen Pengoksidaan: Kekuatan halogen sebagai agen pengoksidaan menurun apabila kita bergerak ke bawah kumpulan. Ini kerana atom menjadi lebih besar dan sukar menerima elektron. Susunannya ialah F₂ > Cl₂ > Br₂ > I₂.
Penyesaran Halogen: Halogen yang lebih reaktif boleh menyesarkan halogen yang kurang reaktif daripada larutan halidanya. Ini berlaku kerana halogen yang lebih reaktif lebih mudah menerima elektron berbanding halogen yang kurang reaktif.
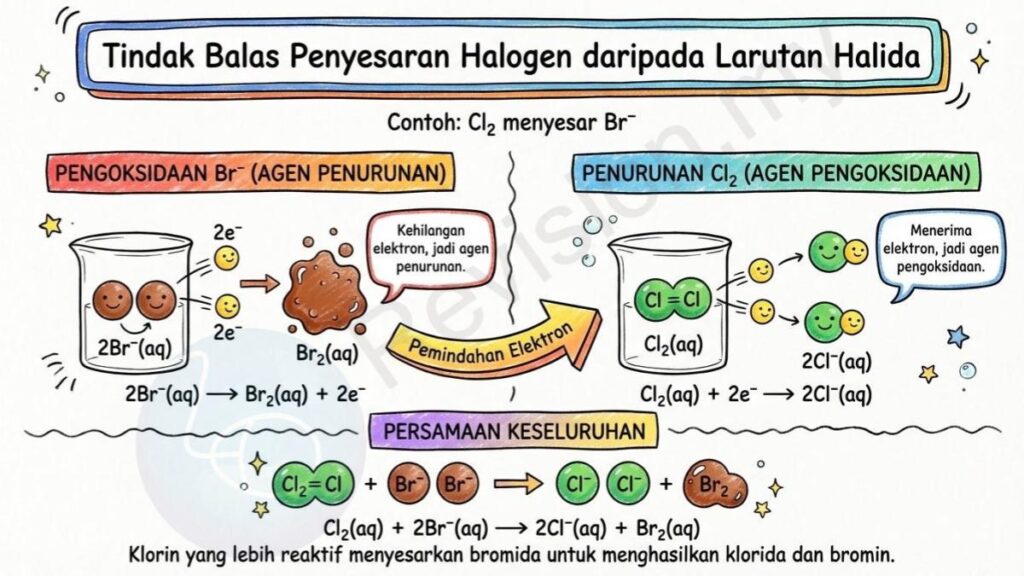
Contoh: Cl₂ menyesar Br⁻
Pengoksidaan Br⁻: 2Br⁻(aq) → Br₂(aq) + 2e⁻. Dalam tindak balas ini, ion bromida kehilangan elektron dan berubah menjadi bromin. Oleh itu, Br⁻ bertindak sebagai agen penurunan kerana ia mendermakan elektron.
Penurunan Cl₂: Cl₂(aq) + 2e⁻ → 2Cl⁻(aq). Molekul klorin pula menerima elektron dan menjadi ion klorida. Oleh sebab itu, Cl₂ bertindak sebagai agen pengoksidaan kerana ia menerima elektron.
Persamaan Keseluruhan: Cl₂(aq) + 2Br⁻(aq) → 2Cl⁻(aq) + Br₂(aq). Persamaan ini menunjukkan bahawa klorin yang lebih reaktif menyesarkan bromida lalu menghasilkan klorida dan bromin sebagai produk akhir.