2.1 Konsep Asas Jirim
Definisi dan Keadaan Fizikal Jirim
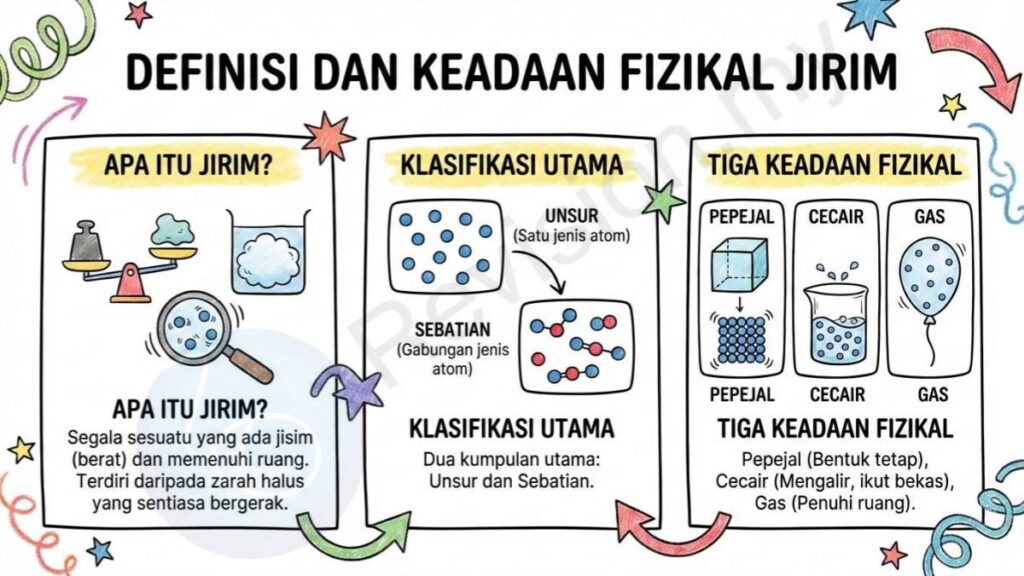
Definisi Jirim: Jirim ialah segala sesuatu yang mempunyai jisim, iaitu berat yang boleh diukur, dan juga mengisi ruang di sekelilingnya. Ia tidak dapat dilihat dengan jelas kerana terdiri daripada zarah-zarah halus yang terlalu kecil untuk dilihat dengan mata kasar. Zarah-zarah ini sentiasa bergerak, sama ada bergetar, berputar, atau bergerak bebas, bergantung kepada keadaan jirim sama ada pepejal, cecair, atau gas.
Klasifikasi Jirim: Semua jirim boleh dikelaskan kepada dua kumpulan utama, iaitu unsur dan sebatian. Pengelasan ini membantu kita memahami bahawa setiap bahan di dunia ini sama ada terdiri daripada satu jenis atom sahaja (unsur) atau gabungan beberapa jenis atom yang berbeza (sebatian). Dengan cara ini, ahli sains dapat mengkaji bagaimana bahan berbeza terbentuk dan bertindak antara satu sama lain.
Keadaan Fizikal: Jirim boleh wujud dalam tiga bentuk utama yang dapat kita lihat dengan jelas, iaitu pepejal, cecair, dan gas. Setiap bentuk mempunyai susunan dan pergerakan zarah yang berbeza. Sebagai contoh, pepejal mempunyai bentuk tetap, cecair boleh mengalir dan mengambil bentuk bekasnya, manakala gas pula bebas memenuhi keseluruhan ruang bekas.
Klasifikasi Jirim: Unsur dan Sebatian
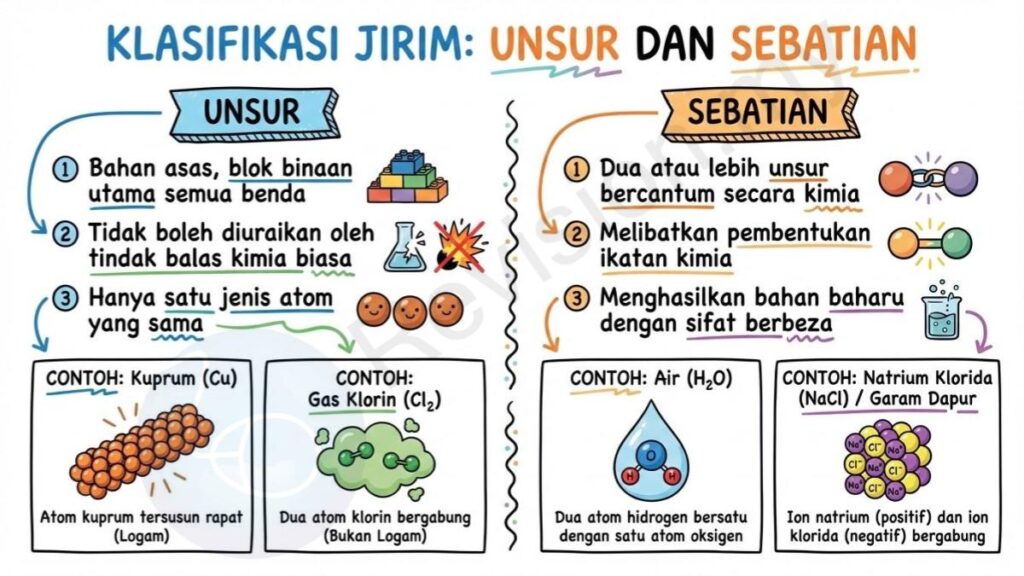
Unsur: Unsur ialah bahan asas yang menjadi blok binaan utama bagi semua benda di sekeliling kita. Ia tidak boleh diuraikan lagi kepada bahan lain melalui tindak balas kimia biasa. Setiap unsur hanya mengandungi satu jenis atom yang sama, dan sifatnya unik serta berbeza daripada unsur lain. Contohnya, emas, oksigen, dan kuprum semuanya ialah unsur yang tidak boleh dipecahkan kepada bahan yang lebih kecil melalui tindak balas kimia.
Contoh Unsur: Contoh bagi unsur termasuk logam seperti kuprum (Cu) yang terdiri daripada atom-atom kuprum yang tersusun rapat. Bagi unsur bukan logam pula, gas klorin (Cl₂) ialah contoh di mana dua atom klorin bergabung membentuk satu molekul unsur. Ini menunjukkan bahawa unsur boleh wujud sama ada dalam bentuk atom tunggal atau molekul yang mengandungi jenis atom yang sama.
Sebatian: Sebatian pula ialah bahan yang terbentuk apabila dua atau lebih unsur bercantum secara kimia. Proses ini melibatkan pembentukan ikatan kimia antara atom-atom unsur yang berbeza untuk menghasilkan bahan baharu dengan sifat yang berbeza daripada unsur asalnya. Sebagai contoh, apabila atom hidrogen bergabung dengan atom oksigen, ia menghasilkan air yang mempunyai sifat yang sangat berbeza daripada kedua-dua gas asal itu.
Contoh Sebatian: Antara contoh sebatian termasuk air (H₂O), yang terbentuk apabila dua atom hidrogen bersatu dengan satu atom oksigen melalui ikatan kimia. Satu lagi contoh ialah natrium klorida (NaCl), atau lebih dikenali sebagai garam dapur, yang terbentuk daripada ion natrium bercas positif dan ion klorida bercas negatif. Gabungan ion-ion ini menghasilkan bahan pepejal yang stabil dan penting dalam kehidupan harian.
Jenis Zarah yang Membentuk Jirim
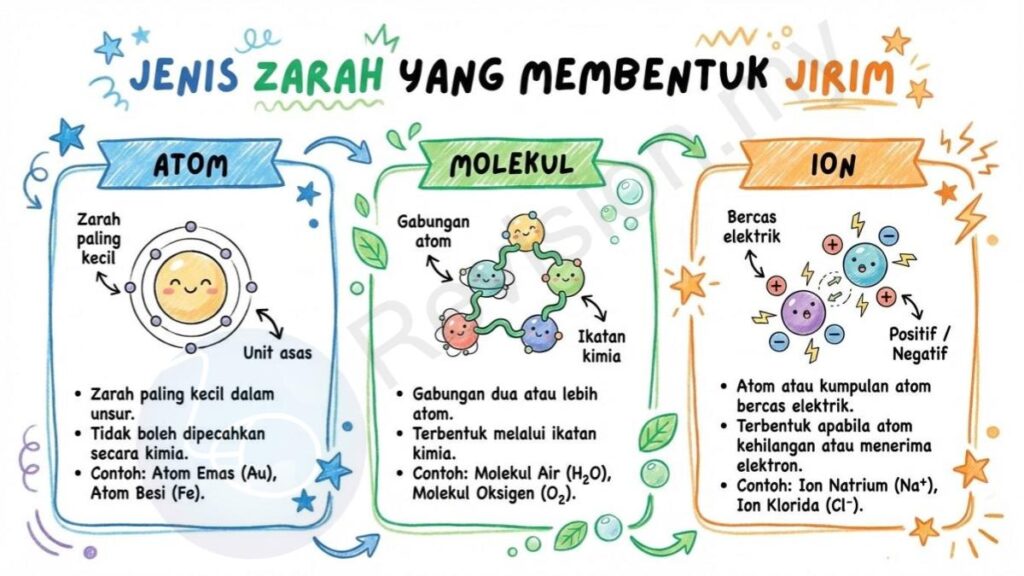
Tiga Jenis Zarah: Semua jirim di alam ini sebenarnya terdiri daripada tiga jenis zarah utama iaitu atom, molekul, dan ion. Setiap jenis zarah mempunyai ciri dan peranan yang berbeza dalam membentuk bahan-bahan yang kita lihat dan gunakan setiap hari. Atom ialah zarah paling kecil, molekul ialah gabungan beberapa atom, manakala ion ialah atom atau kumpulan atom yang mempunyai cas elektrik.
Atom
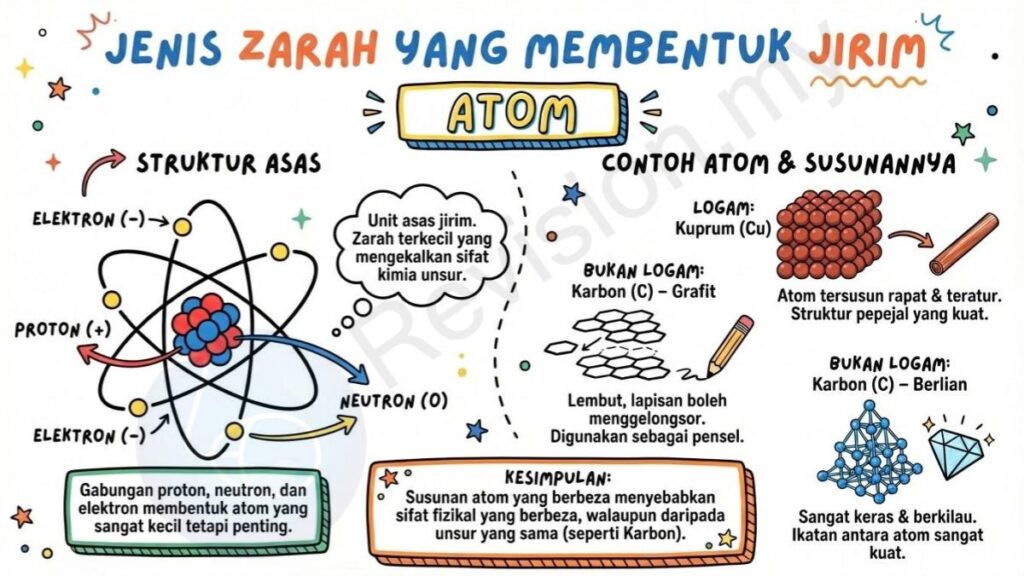
Zarah Paling Ringkas: Atom ialah unit asas bagi semua jirim dan dianggap sebagai zarah terkecil yang masih mengekalkan sifat kimia sesuatu unsur. Ia terdiri daripada tiga jenis zarah subatom iaitu proton, neutron, dan elektron. Proton dan neutron terletak di dalam nukleus di tengah-tengah atom, manakala elektron bergerak mengelilinginya. Gabungan ketiga-tiga zarah ini menjadikan atom sangat kecil tetapi sangat penting dalam pembentukan semua bahan di dunia.
Contoh Atom: Contoh bahan yang terdiri daripada atom termasuk logam seperti kuprum (Cu), yang mempunyai atom tersusun rapat dalam corak yang teratur dan menghasilkan struktur pepejal yang kuat. Bagi bukan logam pula, contoh seperti grafit dan berlian menunjukkan bahawa walaupun kedua-duanya terdiri daripada atom karbon, cara atom-atom tersebut tersusun berbeza menyebabkan sifat fizikalnya juga berbeza. Grafit lembut dan boleh digunakan sebagai pensel, manakala berlian keras dan berkilau kerana ikatan antara atomnya sangat kuat.
Molekul
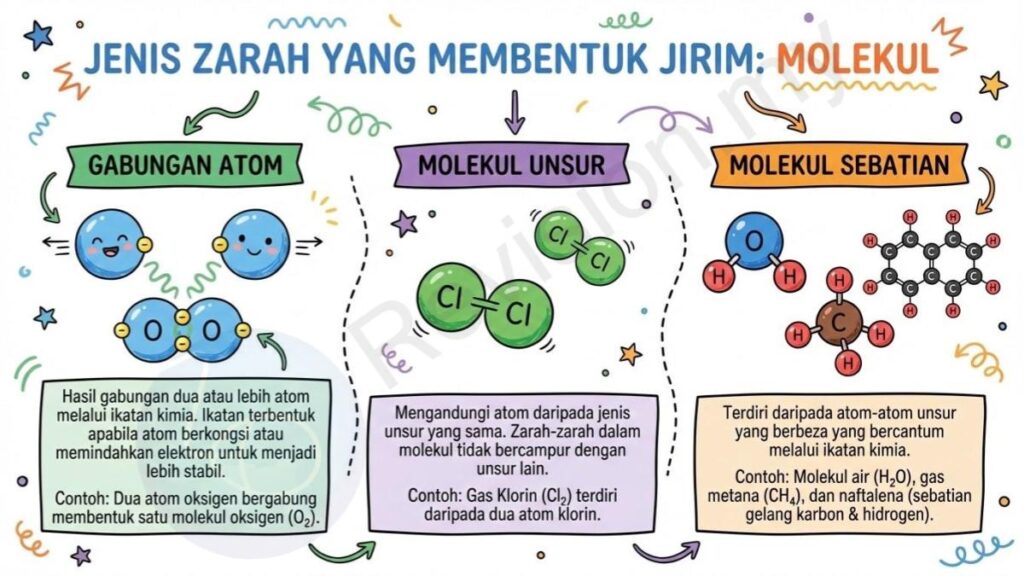
Gabungan Atom: Molekul ialah hasil gabungan dua atau lebih atom yang bersatu melalui ikatan kimia. Ikatan ini terbentuk apabila atom berkongsi atau memindahkan elektron supaya menjadi lebih stabil. Sebagai contoh, dua atom oksigen boleh bergabung untuk membentuk satu molekul oksigen (O₂).
Molekul Unsur: Molekul unsur ialah molekul yang hanya mengandungi atom daripada jenis unsur yang sama. Ini bermakna zarah-zarah dalam molekul tersebut tidak bercampur dengan unsur lain. Contohnya, gas klorin (Cl₂) terdiri daripada dua atom klorin yang bergabung secara kimia.
Molekul Sebatian: Molekul sebatian pula terdiri daripada atom-atom unsur yang berbeza yang bercantum melalui ikatan kimia. Contohnya, molekul air (H₂O) terbentuk apabila dua atom hidrogen bergabung dengan satu atom oksigen. Begitu juga, gas metana (CH₄) mengandungi satu atom karbon dan empat atom hidrogen. Naftalena pula ialah sebatian yang mempunyai banyak atom karbon dan hidrogen yang tersusun dalam bentuk gelang.
Ion
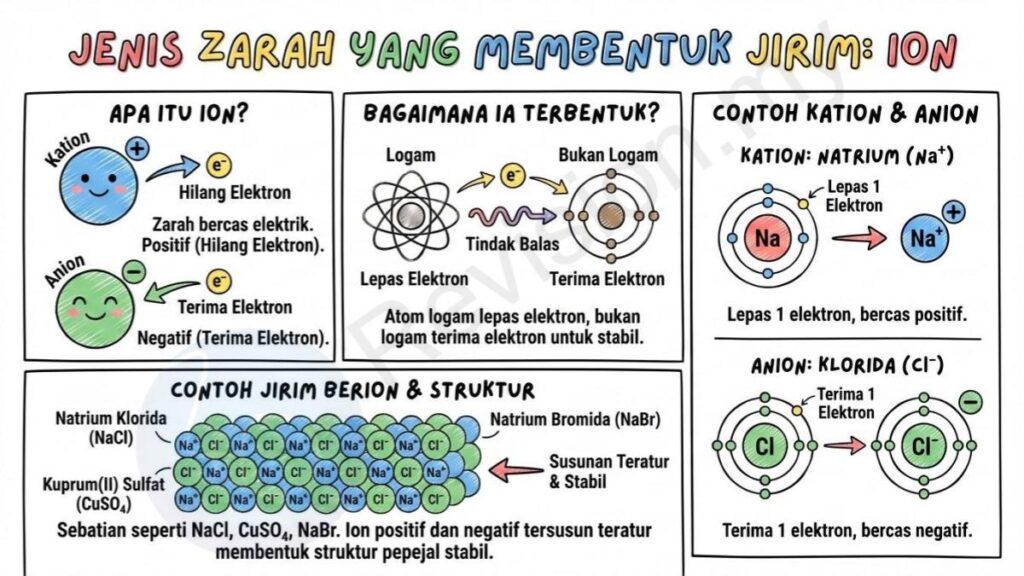
Zarah Bercas: Ion ialah zarah yang mempunyai cas elektrik, sama ada positif atau negatif. Jika zarah kehilangan elektron, ia menjadi bercas positif dan dinamakan kation. Sebaliknya, jika zarah menerima elektron tambahan, ia menjadi bercas negatif dan dinamakan anion.
Terbentuk dari Unsur: Ion terbentuk apabila unsur logam bertindak balas dengan bukan logam. Dalam tindak balas ini, atom logam cenderung melepaskan elektron manakala bukan logam cenderung menerima elektron supaya kedua-duanya mencapai kestabilan tenaga.
Contoh Kation: Ion natrium (Na⁺) ialah contoh kation. Ia terbentuk apabila atom natrium melepaskan satu elektron daripada lapisan luarannya. Kehilangan elektron menyebabkan natrium mempunyai lebih banyak proton daripada elektron, menjadikannya bercas positif.
Contoh Anion: Ion klorida (Cl⁻) ialah contoh anion. Ia terbentuk apabila atom klorin menerima satu elektron tambahan. Penambahan elektron ini menyebabkan atom mempunyai lebih banyak elektron daripada proton, menjadikannya bercas negatif.
Contoh Jirim Berion: Sebatian seperti natrium klorida (NaCl), kuprum(II) sulfat (CuSO₄), dan natrium bromida (NaBr) ialah contoh jirim yang terbentuk daripada ion. Dalam bahan ini, ion positif dan ion negatif disusun secara teratur untuk membentuk struktur pepejal yang stabil dan kukuh.
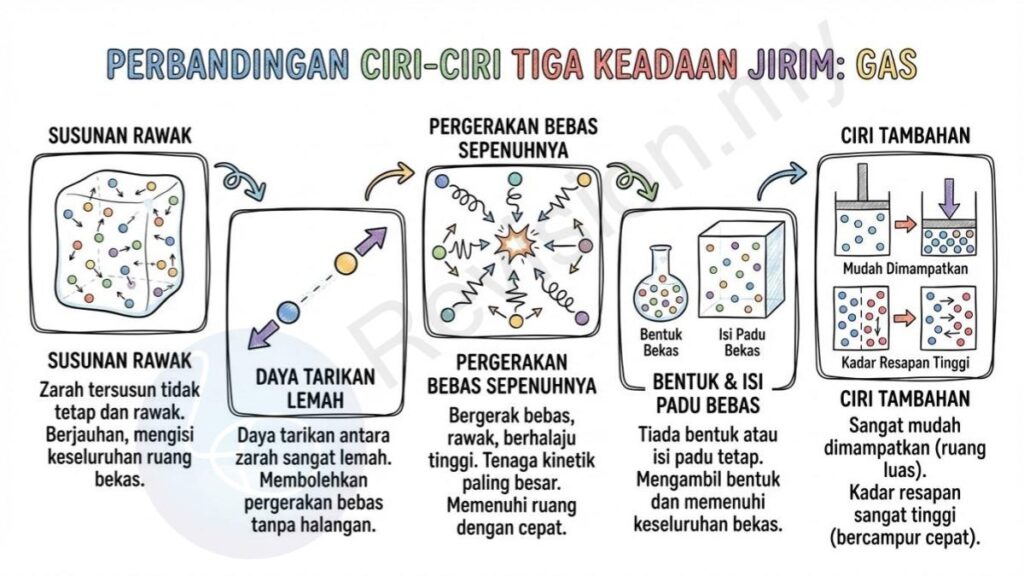
Perbandingan Ciri-Ciri Tiga Keadaan Jirim
Pepejal
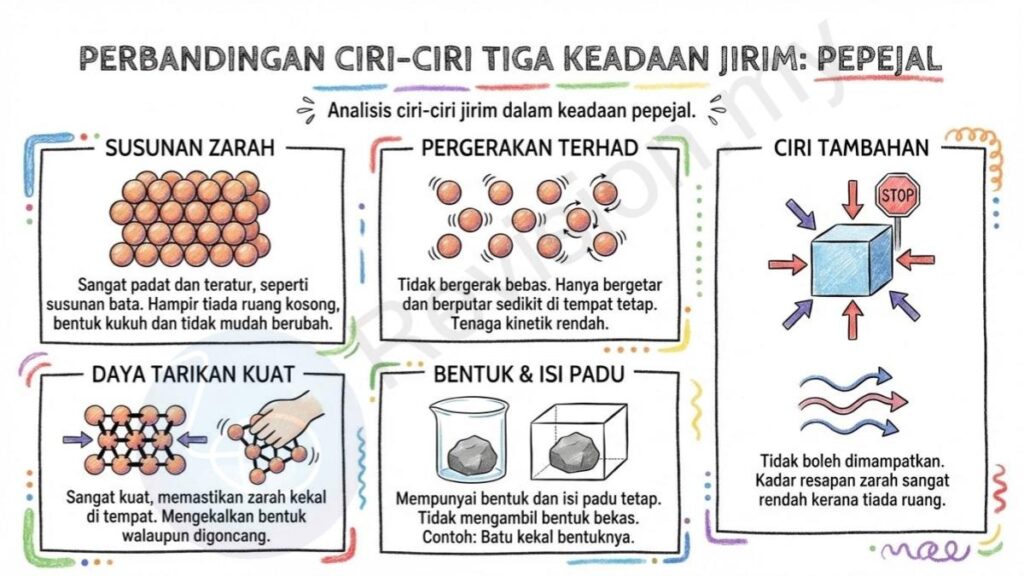
Susunan Zarah: Dalam keadaan pepejal, zarah-zarahnya tersusun dengan sangat padat dan teratur seperti susunan bata di dalam dinding. Hampir tiada ruang kosong antara zarah, menyebabkan pepejal mempunyai bentuk yang kukuh dan tidak mudah berubah.
Daya Tarikan Kuat: Daya tarikan antara zarah dalam pepejal sangat kuat. Daya ini memastikan setiap zarah kekal di tempatnya dan tidak bergerak jauh antara satu sama lain. Itulah sebabnya pepejal mengekalkan bentuknya walaupun digoncang atau dipindahkan.
Pergerakan Terhad: Zarah dalam pepejal tidak boleh bergerak bebas seperti dalam cecair atau gas. Mereka hanya mampu bergetar dan berputar sedikit di tempat tetap. Ini menunjukkan tenaga kinetik mereka rendah kerana pergerakan sangat terbatas.
Bentuk & Isi Padu: Pepejal mempunyai bentuk dan isi padu yang tetap. Ia tidak akan mengambil bentuk bekas kerana zarahnya dikunci rapat oleh daya tarikan kuat. Sebagai contoh, sekeping batu akan kekal bentuknya sama walaupun diletakkan di dalam bekas berbeza.
Ciri Tambahan: Pepejal tidak boleh dimampatkan kerana zarahnya sudah terlalu rapat. Selain itu, kadar resapan zarah dalam pepejal sangat rendah kerana hampir tiada ruang untuk zarah bergerak menembusi antara satu sama lain.
Cecair
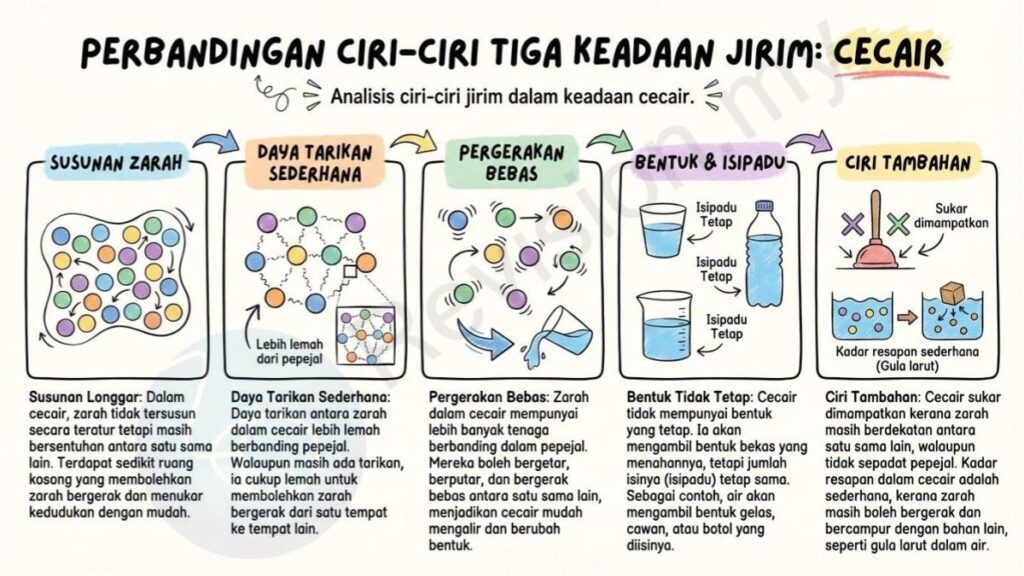
Susunan Longgar: Dalam cecair, zarah tidak tersusun secara teratur tetapi masih bersentuhan antara satu sama lain. Terdapat sedikit ruang kosong yang membolehkan zarah bergerak dan menukar kedudukan dengan mudah.
Daya Tarikan Sederhana: Daya tarikan antara zarah dalam cecair lebih lemah berbanding pepejal. Walaupun masih ada tarikan, ia cukup lemah untuk membolehkan zarah bergerak dari satu tempat ke tempat lain.
Pergerakan Bebas: Zarah dalam cecair mempunyai lebih banyak tenaga berbanding dalam pepejal. Mereka boleh bergetar, berputar, dan bergerak bebas antara satu sama lain, menjadikan cecair mudah mengalir dan berubah bentuk.
Bentuk Tidak Tetap: Cecair tidak mempunyai bentuk yang tetap. Ia akan mengambil bentuk bekas yang menahannya, tetapi jumlah isinya (isipadu) tetap sama. Sebagai contoh, air akan mengambil bentuk gelas, cawan, atau botol yang diisinya.
Ciri Tambahan: Cecair sukar dimampatkan kerana zarah masih berdekatan antara satu sama lain, walaupun tidak sepadat pepejal. Kadar resapan dalam cecair adalah sederhana, kerana zarah masih boleh bergerak dan bercampur dengan bahan lain, seperti gula larut dalam air.
Gas
Susunan Rawak: Dalam keadaan gas, zarah-zarahnya tersusun secara tidak tetap dan rawak. Setiap zarah berjauhan antara satu sama lain kerana daya tarikan antara mereka sangat lemah. Ini menyebabkan gas dapat mengisi keseluruhan ruang yang ada di dalam bekas tanpa bentuk yang tertentu.
Daya Tarikan Lemah: Zarah-zarah gas hampir tidak mempunyai daya tarikan antara satu sama lain. Oleh sebab itu, zarah boleh bergerak bebas ke semua arah tanpa halangan. Daya tarikan yang lemah ini menjadikan gas mudah mengembang dan sukar dikawal bentuknya.
Pergerakan Bebas Sepenuhnya: Zarah dalam gas bergerak dengan bebas dan secara rawak dalam semua arah. Mereka bergerak dengan halaju yang tinggi serta mempunyai tenaga kinetik yang paling besar berbanding zarah dalam pepejal atau cecair. Inilah sebab mengapa gas boleh memenuhi seluruh ruang bekas dengan cepat.
Bentuk & Isi Padu Bebas: Gas tidak mempunyai bentuk tetap seperti pepejal, dan tidak mempunyai isi padu tetap seperti cecair. Sebaliknya, gas akan mengambil bentuk dan memenuhi keseluruhan bekas yang menahannya, tidak kira saiz bekas itu besar atau kecil.
Ciri Tambahan: Gas sangat mudah dimampatkan kerana terdapat ruang yang luas antara zarah-zarahnya. Selain itu, kadar resapan gas juga sangat tinggi, bermaksud gas boleh bercampur dengan cepat dengan gas lain di sekelilingnya.
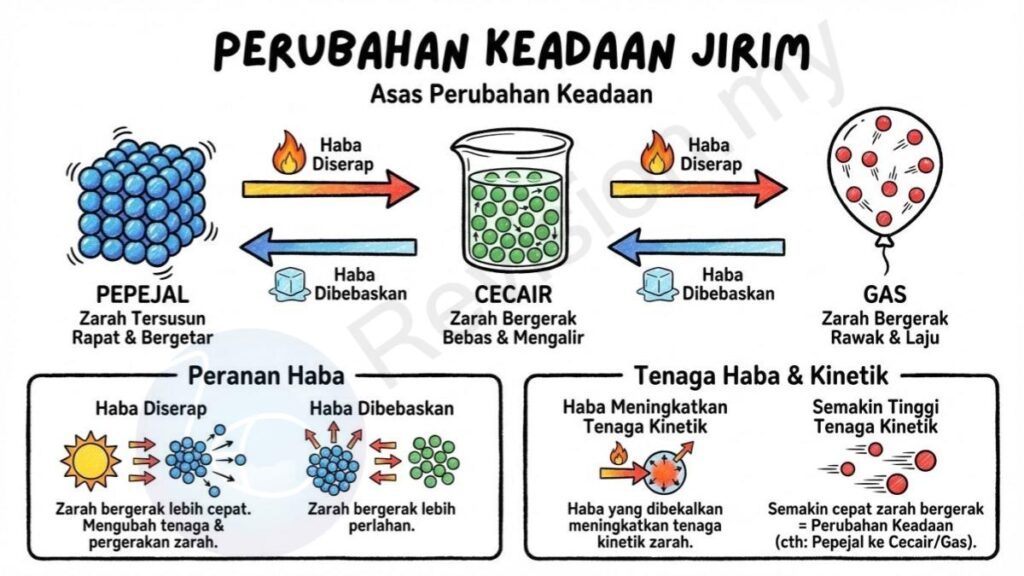
Perubahan Keadaan Jirim
Asas Perubahan Keadaan
Peranan Haba: Perubahan keadaan jirim berlaku apabila haba sama ada diserap atau dibebaskan oleh bahan. Proses ini akan mengubah tenaga dan pergerakan zarah di dalam jirim. Apabila haba diserap, zarah bergerak lebih cepat, manakala apabila haba dibebaskan, zarah bergerak lebih perlahan.
Tenaga Haba: Haba yang dibekalkan kepada jirim sebenarnya meningkatkan tenaga kinetik zarah. Semakin tinggi tenaga kinetik, semakin cepat zarah bergerak, menyebabkan jirim berubah dari pepejal ke cecair atau dari cecair ke gas.
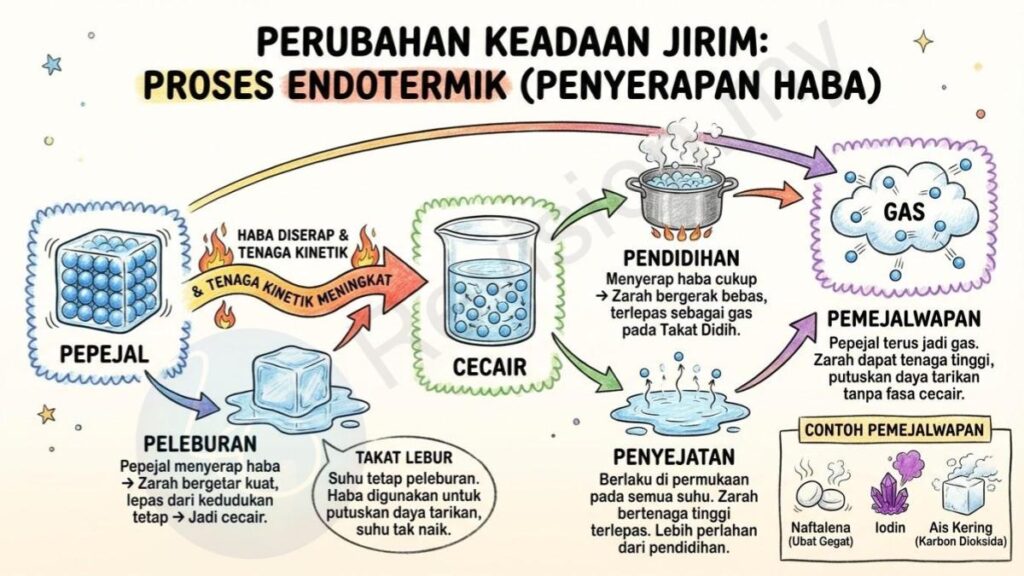
Proses Endotermik (Penyerapan Haba)
Peleburan: Dalam proses ini, pepejal menyerap sejumlah haba daripada persekitaran. Haba yang diterima meningkatkan tenaga kinetik zarah-zarahnya sehingga mereka mula bergetar dengan lebih kuat dan berjaya melepaskan diri daripada kedudukan asal yang tetap. Akhirnya, pepejal berubah menjadi cecair apabila mencapai takat lebur.
Takat Lebur: Takat lebur ialah suhu tertentu di mana pepejal mula mencair. Pada ketika ini, walaupun haba terus dibekalkan, suhu tidak meningkat kerana tenaga tersebut digunakan untuk memutuskan daya tarikan antara zarah-zarah pepejal agar ia boleh menjadi cecair.
Pendidihan: Proses pendidihan berlaku apabila cecair menyerap haba yang mencukupi sehingga zarah-zarahnya memperoleh tenaga untuk bergerak bebas dan terlepas ke udara sebagai gas. Ini berlaku pada suhu tertentu yang dikenali sebagai takat didih, dan pada tahap ini cecair mula bertukar menjadi wap sepenuhnya.
Penyejatan: Penyejatan ialah proses perubahan cecair menjadi gas yang boleh berlaku pada semua suhu, bukan hanya pada takat didih. Ia biasanya berlaku di permukaan cecair apabila zarah-zarah yang mempunyai tenaga tinggi berjaya meninggalkan permukaan untuk menjadi gas. Oleh itu, penyejatan berlaku lebih perlahan berbanding pendidihan.
Pemejalwapan: Pemejalwapan ialah proses di mana pepejal berubah terus menjadi gas tanpa melalui keadaan cecair terlebih dahulu. Ini kerana zarah pepejal memperoleh tenaga yang sangat tinggi sehingga daya tarikan antara mereka dapat diputuskan sepenuhnya tanpa melalui fasa cecair.
Contoh Pemejalwapan: Beberapa bahan seperti naftalena, iodin, dan ais kering (karbon dioksida pepejal) mengalami pemejalwapan apabila dipanaskan. Contohnya, apabila ketulan naftalena dibiarkan di tempat terbuka, ia perlahan-lahan mengecil kerana zarahnya berubah terus menjadi wap.
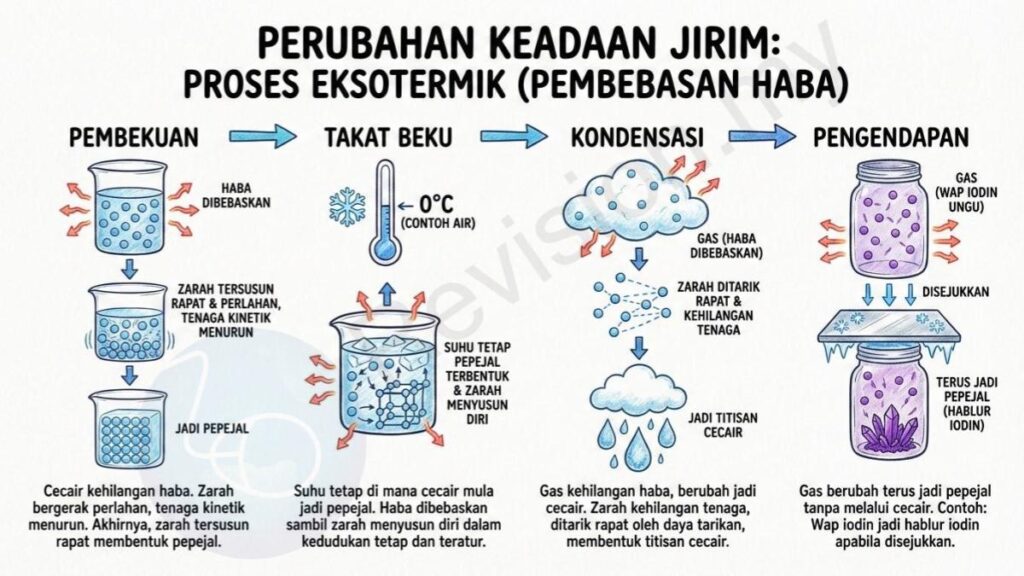
Proses Eksotermik (Pembebasan Haba)
Pembekuan: Ketika proses ini berlaku, cecair kehilangan haba ke persekitaran. Zarah-zarahnya mula bergerak dengan lebih perlahan dan tenaga kinetik mereka menurun. Akhirnya, zarah tersusun rapat dan membentuk pepejal apabila tenaga haba berkurang dengan ketara.
Takat Beku: Takat beku ialah suhu tetap di mana cecair mula bertukar menjadi pepejal. Pada suhu ini, tenaga haba dalam cecair dibebaskan ke persekitaran sambil zarah-zarah menyusun diri dalam kedudukan yang tetap dan teratur.
Kondensasi: Proses ini berlaku apabila gas kehilangan haba dan berubah menjadi cecair. Zarah-zarah gas yang bergerak bebas mula kehilangan tenaga, lalu ditarik rapat oleh daya tarikan antara mereka sehingga membentuk titisan cecair.
Pengendapan: Pengendapan ialah proses di mana gas berubah terus menjadi pepejal tanpa melalui keadaan cecair. Sebagai contoh, wap iodin boleh bertukar semula menjadi hablur iodin pepejal apabila disejukkan.
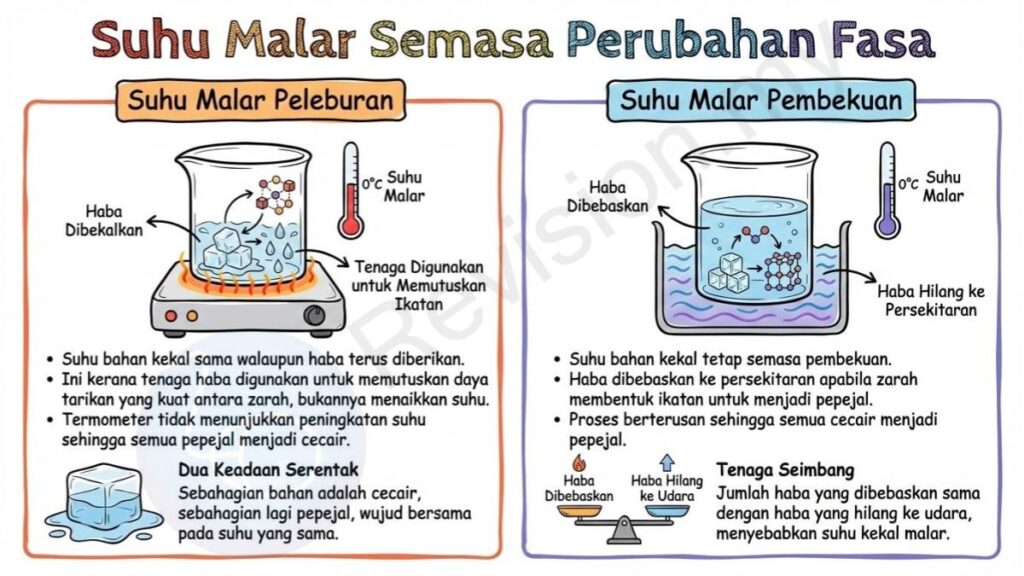
Suhu Malar Semasa Perubahan Fasa
Suhu Malar Peleburan: Suhu bahan kekal sama walaupun haba terus diberikan. Ini kerana tenaga haba yang diterima digunakan sepenuhnya untuk memutuskan daya tarikan yang kuat antara zarah dalam pepejal, bukannya untuk menaikkan suhu. Akibatnya, walaupun bahan menyerap haba, termometer tidak menunjukkan peningkatan suhu sehingga semua zarah terpisah dan bahan menjadi cecair sepenuhnya.
Dua Keadaan Serentak: Ketika proses peleburan sedang berlaku, sebahagian bahan sudah menjadi cecair manakala sebahagian lagi masih pepejal. Kedua-dua keadaan ini wujud bersama pada suhu yang sama sehingga keseluruhan bahan selesai berubah menjadi cecair.
Suhu Malar Pembekuan: Semasa pembekuan, suhu bahan juga kekal tetap. Hal ini kerana tenaga haba dalam bahan dibebaskan ke persekitaran apabila zarah mula membentuk ikatan rapat untuk menjadi pepejal. Proses ini berterusan sehingga semua zarah tertarik rapat dan membentuk struktur pepejal sepenuhnya.
Tenaga Seimbang: Dalam proses pembekuan, jumlah tenaga haba yang keluar daripada bahan adalah sama dengan tenaga yang hilang ke udara sekeliling. Keseimbangan ini menyebabkan suhu kekal malar sepanjang proses berlaku.
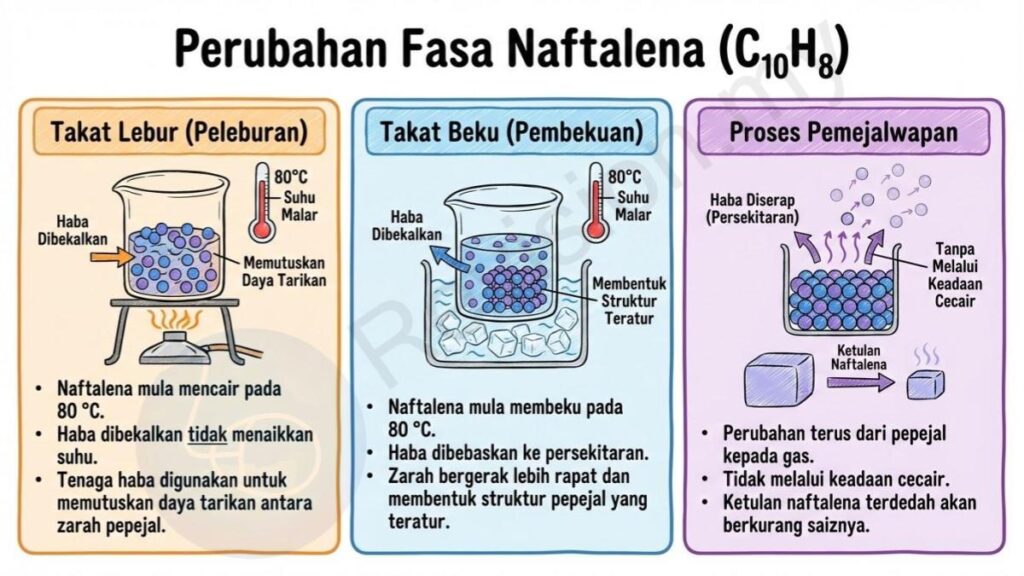
Contoh Bahan: Naftalena (C₁₀H₈)
Takat Lebur Naftalena: Naftalena mula mencair pada suhu 80 °C. Pada ketika ini, haba yang dibekalkan tidak menaikkan suhu, sebaliknya membantu memutuskan daya tarikan antara zarah pepejal supaya ia berubah menjadi cecair.
Takat Beku Naftalena: Naftalena juga mula membeku pada suhu yang sama, iaitu 80 °C. Semasa ini, haba dibebaskan apabila zarah bergerak lebih rapat dan membentuk struktur pepejal yang teratur.
Proses Pemejalwapan: Naftalena mempunyai keistimewaan boleh bertukar terus daripada pepejal kepada gas tanpa melalui keadaan cecair. Proses ini dinamakan pemejalwapan, dan ia boleh dilihat apabila ketulan naftalena yang dibiarkan terdedah lama akan berkurang saiznya kerana zarah pepejal terus berubah menjadi gas.