9.2 Potensi Elektrod Piawai
Keupayaan Elektrod (KE)
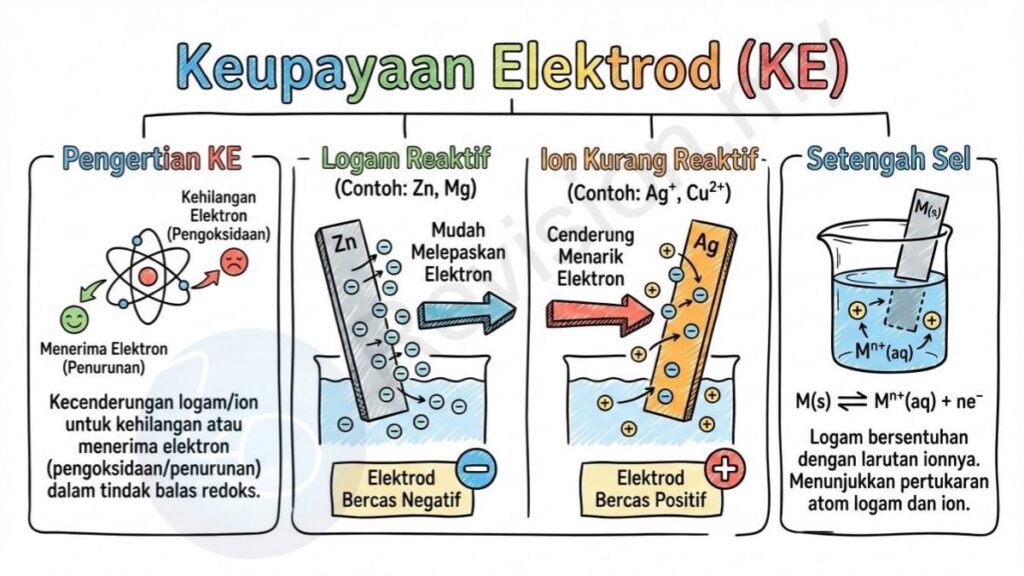
Pengertian KE: KE ialah kecenderungan logam atau ion untuk kehilangan elektron (menjalani pengoksidaan) atau menerima elektron (menjalani penurunan). Ini membantu kita memahami bagaimana sesuatu bahan bertindak dalam tindak balas redoks.
Logam Reaktif: Logam seperti zink (Zn) dan magnesium (Mg) sangat reaktif kerana mereka mudah melepaskan elektron. Oleh sebab itu, elektrod yang terbentuk daripadanya menjadi bercas negatif.
Ion Kurang Reaktif: Ion seperti Ag⁺ dan Cu²⁺ tidak mudah kehilangan elektron, sebaliknya lebih cenderung menarik elektron daripada bahan lain, menjadikan elektrod yang terhasil bercas positif.
Setengah Sel: Satu setengah sel terbentuk apabila logam bersentuhan dengan larutan ionnya. Hubungan ini dinyatakan sebagai M(s) ⇌ Mⁿ⁺(aq) + ne⁻, menunjukkan pertukaran antara atom logam dan ionnya.
Keupayaan Elektrod Piawai (E°)
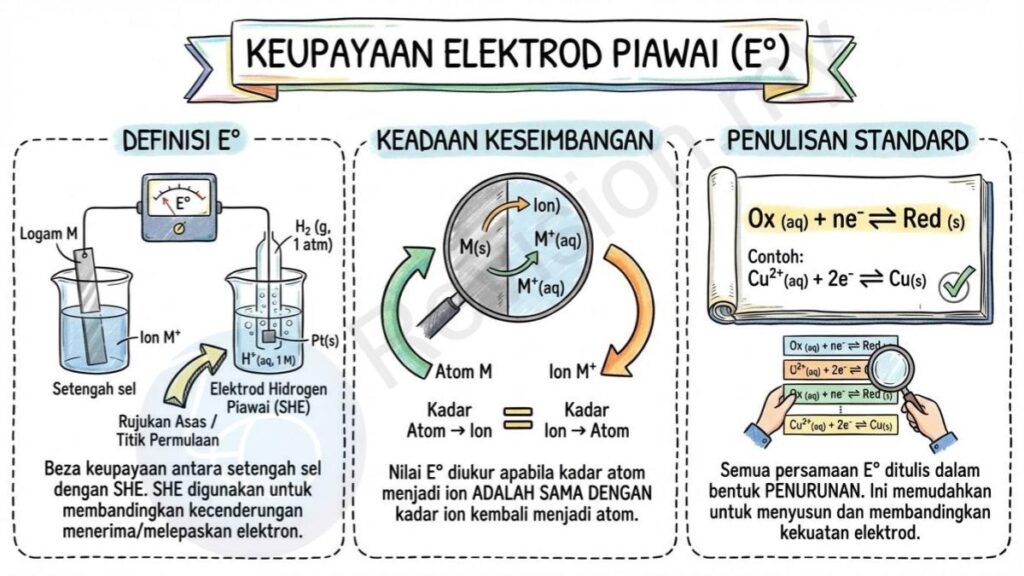
Definisi E°: Keupayaan elektrod piawai ialah beza keupayaan antara sesuatu setengah sel dengan elektrod hidrogen piawai (SHE), yang digunakan sebagai rujukan asas. Ini bermaksud SHE menjadi titik permulaan yang membolehkan kita membandingkan kecenderungan pelbagai logam untuk menerima atau melepaskan elektron.
Keadaan Keseimbangan: Nilai E° diukur apabila keadaan keseimbangan berlaku antara atom logam dan ion logam dalam setengah sel tersebut, iaitu ketika kadar atom menjadi ion adalah sama dengan kadar ion kembali menjadi atom.
Penulisan Standard: Semua setengah persamaan E° ditulis dalam bentuk penurunan kerana cara ini memudahkan untuk menyusun, membaca, dan membandingkan kekuatan pelbagai elektrod.
Syarat Piawai Pengukuran
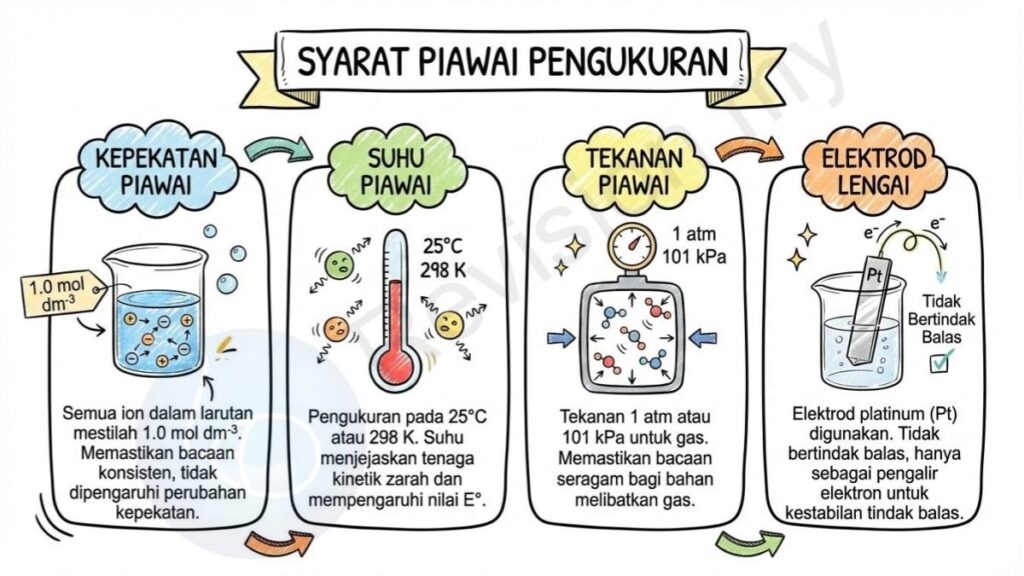
Kepekatan Piawai: Semua ion dalam larutan mestilah mempunyai kepekatan 1.0 mol dm⁻³ supaya bacaan keupayaan elektrod adalah konsisten dan tidak dipengaruhi oleh perubahan kepekatan larutan.
Suhu Piawai: Pengukuran dilakukan pada suhu 25°C atau 298 K kerana suhu boleh menjejaskan tenaga kinetik zarah dan seterusnya mempengaruhi nilai E°.
Tekanan Piawai: Tekanan 1 atm atau 101 kPa digunakan untuk gas supaya bacaan keupayaan elektrod bagi bahan yang melibatkan gas adalah seragam dan boleh dibandingkan antara eksperimen.
Elektrod Lengai: Elektrod platinum digunakan apabila logam tidak terlibat secara langsung dalam setengah sel kerana platinum tidak bertindak balas dan hanya berfungsi sebagai pengalir elektron bagi memastikan tindak balas dapat berlaku dengan stabil.
Elektrod Hidrogen Piawai (SHE)
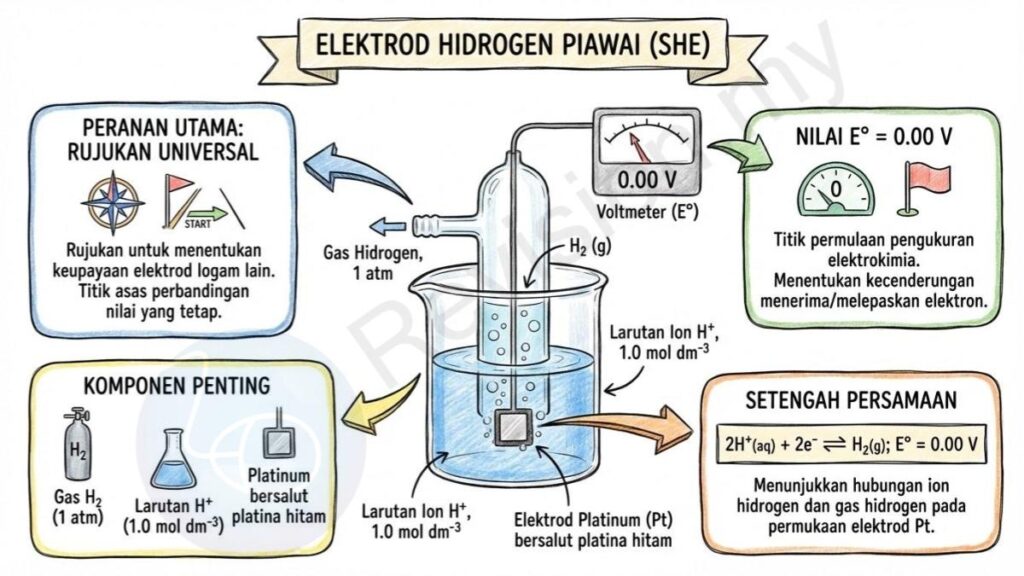
Peranan SHE: Elektrod hidrogen piawai digunakan sebagai rujukan universal untuk menentukan keupayaan elektrod bagi logam lain. Ini bermaksud SHE menjadi titik asas untuk membandingkan semua elektrod kerana ia memberikan nilai yang tetap dan boleh dipercayai.
Nilai E° SHE: Nilai E° SHE ditetapkan sebagai 0.00 V, menjadikannya titik permulaan untuk semua pengukuran elektrokimia. Dengan nilai sifar ini, saintis dapat menentukan sama ada sesuatu elektrod lebih mudah menerima atau melepaskan elektron berbanding SHE.
Komponen SHE: SHE terdiri daripada gas hidrogen pada tekanan 1 atm, larutan ion H⁺ dengan kepekatan 1.0 mol dm⁻³, dan elektrod platinum yang disalut platina hitam untuk meningkatkan luas permukaan. Setiap komponen ini penting supaya tindak balas dapat berlaku dengan stabil dan menghasilkan bacaan yang tepat.
Setengah Persamaan SHE: Persamaan 2H⁺(aq) + 2e⁻ ⇌ H₂(g); E° = 0.00 V menunjukkan hubungan antara ion hidrogen dan gas hidrogen pada elektrod. Persamaan ini menggambarkan bagaimana ion H⁺ menerima elektron untuk membentuk gas hidrogen di permukaan elektrod platinum.
Hubungan E° dengan Kekuatan Agen Redoks
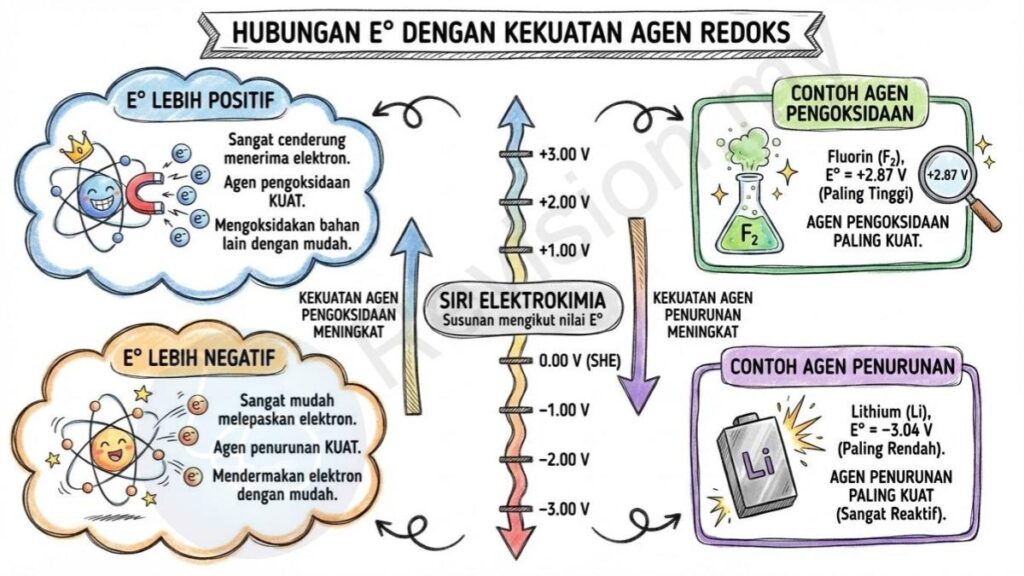
Siri Elektrokimia: Siri elektrokimia ialah satu susunan elektrod yang disusun mengikut nilai E° mereka, bermula daripada nilai paling negatif hingga nilai paling positif. Susunan ini membantu kita meramal sama ada sesuatu tindak balas redoks akan berlaku dan menentukan bahan mana yang lebih mudah menerima atau melepaskan elektron.
E° Lebih Positif: Jika sesuatu elektrod mempunyai nilai E° yang lebih positif, ini menunjukkan bahawa elektrod tersebut sangat cenderung untuk menerima elektron. Oleh itu, ia bertindak sebagai agen pengoksidaan yang kuat kerana ia boleh mengoksidakan bahan lain dengan mudah.
Contoh Agen Pengoksidaan: Fluorin (F₂) mempunyai nilai E° = +2.87 V, iaitu nilai yang paling tinggi dalam siri elektrokimia. Ini menjadikannya agen pengoksidaan paling kuat kerana ia sangat mudah menerima elektron daripada bahan lain.
E° Lebih Negatif: Jika nilai E° bagi sesuatu elektrod sangat negatif, ini menunjukkan bahawa bahan tersebut sangat mudah melepaskan elektron. Oleh itu, ia menjadi agen penurunan yang kuat kerana ia boleh mendermakan elektron kepada bahan lain dengan mudah.
Contoh Agen Penurunan: Lithium (Li) dengan nilai E° = −3.04 V ialah agen penurunan paling kuat dalam siri elektrokimia kerana ia melepaskan elektron dengan sangat mudah, menjadikannya sangat reaktif sebagai logam penurun.
Peramalan Tindak Balas Redoks Spontan
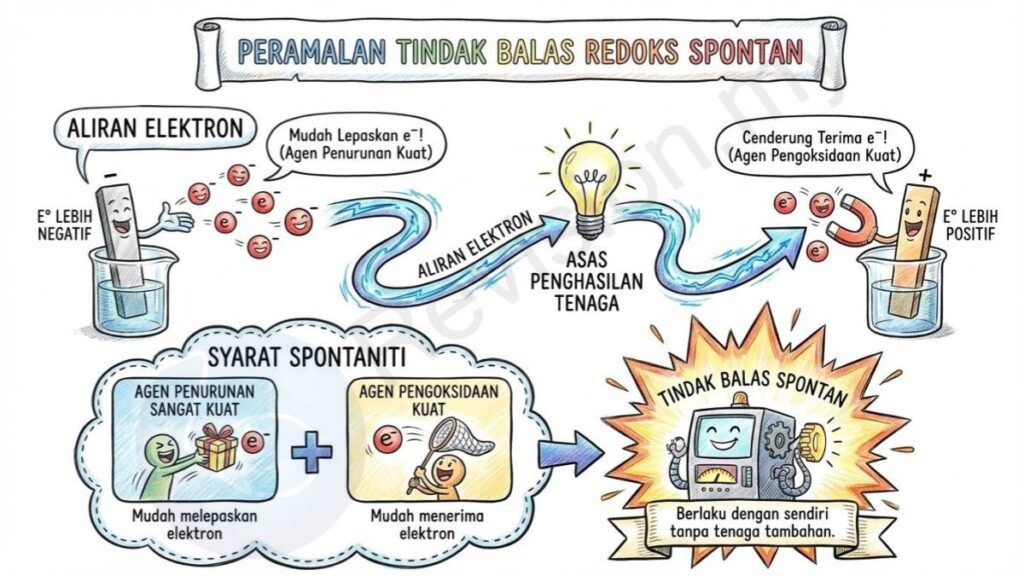
Aliran Elektron: Elektron sentiasa bergerak dari setengah sel yang mempunyai nilai E° lebih negatif kerana bahan tersebut lebih mudah melepaskan elektron, menuju ke setengah sel yang mempunyai nilai E° lebih positif yang lebih cenderung menerima elektron. Pergerakan ini adalah asas kepada cara sel elektrokimia menghasilkan tenaga.
Syarat Spontaniti: Tindak balas redoks berlaku secara spontan apabila terdapat agen penurunan yang sangat kuat yang mudah melepaskan elektron serta agen pengoksidaan yang kuat yang mudah menerima elektron. Apabila kedua-dua syarat ini dipenuhi, tindak balas akan berlaku dengan sendiri tanpa memerlukan tenaga tambahan.
Contoh: Zn dan Cu²⁺
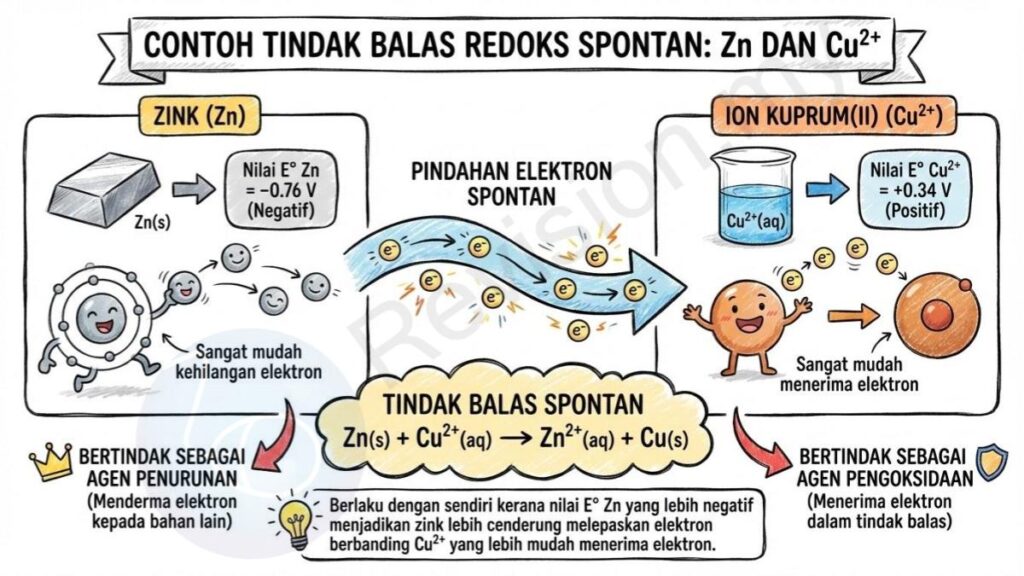
Nilai E° Zn: Nilai E° zink ialah −0.76 V, menunjukkan bahawa zink sangat mudah kehilangan elektron. Oleh itu, ia bertindak sebagai agen penurunan kerana ia menyumbangkan elektron kepada bahan lain.
Nilai E° Cu²⁺: Nilai E° bagi ion kuprum(II) ialah +0.34 V, menunjukkan bahawa Cu²⁺ sangat mudah menerima elektron dan oleh itu bertindak sebagai agen pengoksidaan dalam tindak balas redoks.
Tindak Balas Spontan: Zn(s) + Cu²⁺(aq) → Zn²⁺(aq) + Cu(s); tindak balas ini berlaku dengan sendiri kerana nilai E°Zn yang lebih negatif menjadikan zink lebih cenderung melepaskan elektron berbanding Cu²⁺ yang lebih mudah menerima elektron, menyebabkan tindak balas berlaku secara spontan.